2024년 CAR-T 전립선암 CAR-NK BCMA CAR-T 연구발표
페이지 정보
작성자 PnH 조회109회 작성일 24-07-13 17:05본문
CAR-T (Chimeric Antigen Receptor T-Cell Immunotherapy)는 키메라 항원 수용체 T세포 면역치료제 입니다 .
이 치료법은 수년 동안 사용되어 왔지만 최근 몇 년간 임상적으로 개선되어 사용된 새로운 유형의 세포 치료법입니다.
급성 백혈병 및 비호지킨 림프종 치료에 상당한 효능을 갖고 있으며 가장 최신의 암 치료법 중 모든 기술과 마찬가지로 CAR-T 기술도 오랜 진화 과정을 거쳐 CAR-T 기술이 점차 발전했습니다.
이 치료 전략의 핵심은 표적 세포를 인식하고 환자의 T 세포가 CAR을 발현하도록 유전자 변형된 CAR(키메라 항원 수용체)이라는 인공 수용체입니다. 임상 시험에서 과학자들은 투석과 유사한 과정을 통해 환자로부터 일부 T 세포를 추출한 다음 배양실에서 이를 유전적으로 변형하고 이 T 세포가 이 새로운 수용체를 발현할 수 있도록 이 CAR을 암호화하는 유전자를 배양했습니다. 이러한 유전적으로 변형된 T 세포는 배양실에서 증식된 다음 환자에게 다시 주입됩니다. 이러한 T 세포는 자신이 발현하는 CAR 수용체를 사용하여 표적 세포 표면의 분자에 결합하며, 이 결합은 내부 신호를 유발하여 T 세포를 매우 강력하게 활성화하여 표적 세포를 빠르게 파괴합니다.
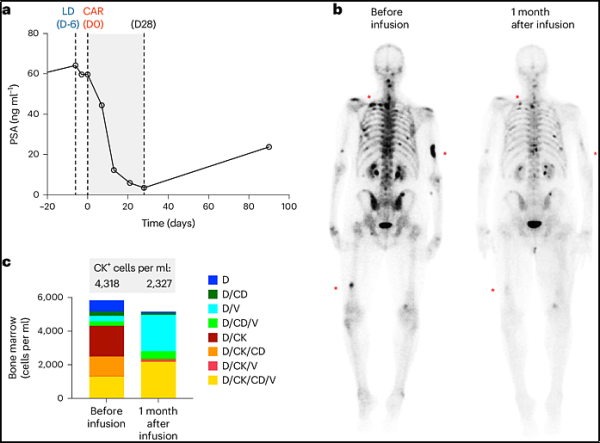
1. Nature Medicine:PSCA-CAR T cell therapy in metastatic castration-resistant prostate cancer: a phase 1 trial
현재 면역요법으로 전립선암을 치료하는 것은 어렵다. 그러나 City of Hope 연구진이 개발한 키메라 항원 수용체(CAR) T 세포(CAR-T) 치료법에 대한 최초의 인간 대상 임상 1상 시험 결과에 따르면 진행성 전립선암 환자가 이 세포 면역 치료법을 안전하게 받을 수 있는 것으로 나타났습니다.
관련 연구 결과는 네이처 메디슨(Nature Medicine) 2024년 6월호에 'PSCA-CAR T cell therapy in metastatic castration-resistant prostate cancer: a phase 1 trial'이라는 제목으로 게재됐습니다.
Nature Medicine, 2024, doi:10.1038/s41591-024-02979-8
이 임상시험에서는 전립선 줄기세포 항원(PSCA) 양성 전이성 거세저항성 전립선암(mCRPC) 환자 14명을 치료하기 위해 CAR-T 세포 치료법을 사용했습니다 . 세포가 전립선 밖으로 퍼져 더 이상 호르몬 치료에 반응하지 않습니다. 미국에서는 매년 이 유형의 전립선암에 걸린 남성 34,000명 이상이 사망합니다.
논문의 공동 교신저자이자 City of Hope 혈액학 및 조혈 세포 이식학과 부교수인 Saul Priceman 박사와 그의 팀은 전립선암에서 많이 발현되는 PSCA를 표적으로 하는 CAR-T 세포를 개발했습니다. 이 치료법은 혈액에서 환자의 면역세포(T세포라고 함)를 추출하고, CAR을 이용해 추출한 T세포를 실험실에서 리프로그래밍해 암세포 표면의 PSCA 단백질을 인식하고 공격할 수 있도록 하는 치료법입니다. 이렇게 재프로그래밍된 CAR-T 세포는 환자에게 다시 주입되어 암세포를 파괴합니다.
공동 교신저자이자 논문 제1저자이자 City of Hope의 종양학 및 치료 연구과 교수인 Tanya Dorff 박사는 이렇게 말했습니다. “전립선암은 면역치료의 불모지로 알려져 있습니다. 이 암의 종양 미세 환경은 종양 내에 T 세포가 많지 않기 때문에 이를 극복하려면 매우 강력한 방법이 필요합니다. 우리의 연구에 따르면 City of Hope의 전립선암 CAR-T 세포 치료법은 이에 한 걸음 더 가까워질 수 있습니다. "
2. Cancer Discovery:CD28 costimulation augments CAR signaling in NK cells via the LCK/CD3Z/ZAP70 signaling axis
새로운 연구에서 텍사스 대학교 MD 앤더슨 암 센터의 연구자들은 CD70+ 암을 표적으로 하는 제대혈 유래 키메라 항원 수용체(CAR) 자연살해세포(CAR-NK)를 발현하는 세포에서 CD28 공동자극을 추가하면 암세포의 기능을 크게 향상시킬 수 있음을 발견했습니다. CAR-NK 세포의 항종양 효능 및 장기 세포독성. 이는 혈액암 및 고형 종양의 전임상 모델에서 성숙한 NK 세포에는 일반적으로 존재하지 않는 T 세포에서 주로 발견되는 보조자극 분자인 CD28을 추가하면 CAR-NK의 기능을 향상시킬 수 있음을 보여줌으로써 향후 NK 세포 치료법을 제안합니다. 유전자 변형에 대한 이러한 접근 방식을 고려해야 합니다.
관련 연구 결과는 "CD28 costimulation augments CAR signaling in NK cells via the LCK/CD3Z/ZAP70 signaling axis"라는 제목으로 Cancer Discovery 저널에 2024년 6월 20일 온라인 게재되었습니다.
논문의 교신저자이자 텍사스대학교 MD 앤더슨 암센터 줄기세포 이식 및 세포치료 교수인 카타윤 레즈바니(Katayoun Rezvani) 박사는 “암 치료에 있어서 NK 세포의 선천적인 항종양 활성과 그 잠재력을 바탕으로 표적 항원으로서의 CD70, CD70 표적화 CAR-NK 세포는 많은 고형 종양에 대한 효과적인 치료법이 될 가능성이 있습니다. 다양한 공동자극 분자를 탐색한 후, 우리는 CD28을 추가하는 것이 CAR-NK 세포를 개선하는 가치 있는 접근법이라는 것을 발견했습니다. 지속성과 효능은 좋은 결과가 가능함을 시사합니다.”
CD70 발현은 종양 진행 및 면역 회피에 기여하는 것으로 나타나 CAR-NK 세포 치료의 이상적인 표적이 됩니다. 따라서 Rezvani 연구소의 수석 연구 과학자인 Sunil Acharya 박사와 다른 사람들은 CD70 표적 CAR-NK 세포를 암세포 치료법으로 사용하기 위해 조작하고 최적화하려고 노력하고 있습니다. 이를 달성하기 위해 그들은 CD70에 대한 천연 수용체인 CD27을 CAR-NK 세포에 통합하여 CD70+ 암세포에 결합했습니다. 그들은 또한 CAR-NK 세포 활성을 향상시키기 위해 CD28을 포함하여 CD3ζ와 쌍을 이루는 여러 공동자극 분자를 평가했습니다. 마지막으로 이전 연구 결과에 따르면 이러한 CAR-NK 세포에는 NK 세포 지속성을 증가시키는 IL-15와 안전 스위치로 iC9도 포함되어 있습니다.
CD28 함유 CD70 표적화 CAR-NK 세포는 시험관 내 및 다중 혈액학적 및 고형 종양 모델에서 CD70+ 종양 세포 에 대해 높은 세포독성을 나타냅니다 . CD28은 지속적으로 테스트된 최고의 보조자극 조절 분자 중 하나입니다. 주의 깊은 연구 끝에 이들 저자는 CD28이 CAR-NK 세포에서 LCK, CD3ζ 및 ZAP70과 관련된 주요 신호 전달 경로를 활성화하여 항종양 활성을 향상시키는 것을 발견했습니다.
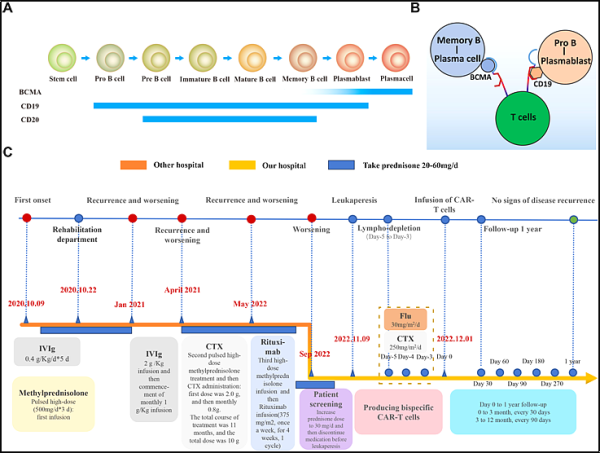
3. hLife:BCMA-CD19 bispecific CAR-T therapy in refractory chronic inflammatory demyelinating polyneuropathy
만성 염증성 탈수초 다발신경병증(CIDP)은 움직임, 감각, 언어, 호흡 및 심박수에 영향을 미치는 신경 손상을 포함한 갑작스러운 증상을 나타내는 흔하지 않은 질병입니다. 환자의 80% 이상에서는 근육 약화, 보행 장애, 힘줄 반사 상실, 감각 상실, 균형 문제가 발생하며, 심한 경우에는 마비, 불규칙한 심장 박동 및 호흡 곤란이 발생합니다. 현재 코르티코스테로이드, 혈장 교환, 정맥 면역글로불린(IVIg) 과 같은 치료법은 증상을 조절하는 데 도움이 될 수 있지만 질병을 완전히 근절할 수는 없습니다.
2024, doi:10.1016/j.hlife.2024.05.005
새로운 연구에서 중국 쉬저우 의과대학 연구진은 CIDP 치료에서 BCMA-CD19 이중특이성 CAR-T 세포의 타당성, 내약성 및 효능을 밝히고 CIDP 치료에서 CAR-T 세포 치료의 잠재력을 강조했습니다. 재발성/불응성 자가면역 질환의 가능성. 이 전략은 CIDP에 대한 치료 가능한 치료법으로 이어질 수 있습니다.
관련 연구 결과는 'BCMA-CD19 bispecific CAR-T therapy in refractory chronic inflammatory demyelinating polyneuropathy'이라는 제목으로 hLife 저널에 2024년 5월 28일자 온라인 게재됐습니다.
형질아세포와 수명이 긴 형질 세포에 BCMA 단백질이 있다는 점을 이용하여, 저자들은 CD19와 BCMA를 모두 표적으로 삼는 이중특이성 CAR-T 세포를 설계했습니다. 이는 B 세포와 형질 세포를 일시적이고 깊게 제거하여 면역 균형을 재설정하는 것을 목표로 합니다.
재발성/불응성 CIDP를 앓고 있는 44세 남성 환자가 말단 사지 무감각 및 을 피로감이 동반되었습니다.
그는 2021년 유럽 신경학회/말초신경학회 CIDP 지침 에 따라 IgG4 자가항체가 없는 원위 CIDP 진단을 받았습니다 . 입원 후 평가와 논의 끝에 자가면역질환 치료를 위한 이중특이성 CAR-T 치료를 받을 수 있는 자격을 얻어 성공적으로 치료를 받았습니다.
CAR-T 세포치료를 받은 후 남성 환자의 기능은 INCAT 장애와 MRC 점수를 기준으로 크게 개선됐습니다. 특히 CAR-T 치료를 받은 지 180일 만에 근력이 거의 완전히 회복돼 다시 걸을 수 있게 됐습다.
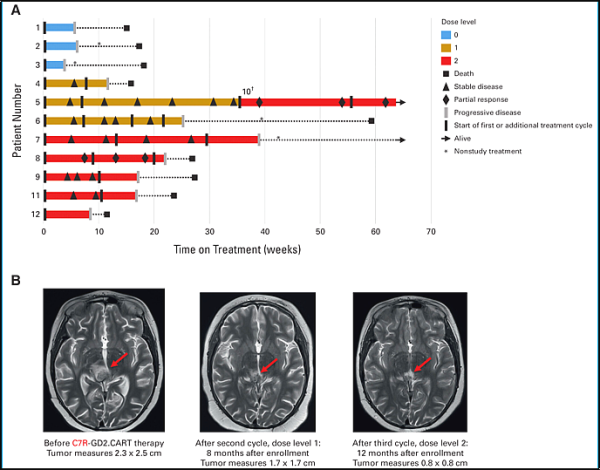
4. Journal of Clinical Oncology:Phase I Trial of GD2.CART Cells Augmented With Constitutive Interleukin-7 Receptor for Treatment of High-Grade Pediatric CNS Tumors
미만성 정중선 신경교종(DMG) 및 기타 재발성 고급 중추신경계 종양은 예후가 좋지 않은 공격적인 뇌암 으로 소아 환자에게 새로운 치료법이 필요합니다. CAR(키메라 항원 수용체) 변형 T 세포(CAR-T)를 사용하는 면역요법은 다른 암에서는 효능을 보였지만 DMG 및 기타 중추신경계 종양에서는 사용이 제한되었습니다.
Journal of Clinical Oncology, 2024, doi:10.1200/JCO.23.02019
새로운 연구에서 텍사스 아동암센터, 베일러 의과대학 세포 및 유전자 치료 센터, 텍사스 아동병원, 휴스턴 메소디스트 병원의 연구원들은 GD2에 대한 DMG 및 강화된 CAR-T 세포 치료법을 표적으로 삼는 약물을 개발했습니다. 다른 중추신경계 종양에서 고도로 발현되는 항원. 텍사스 아동 암 센터의 1상 임상 시험에서 이 치료법은 환자들의 내약성이 좋았으며 일부 환자는 종양 관련 신경학적 결손의 일시적인 개선을 경험하여 이 새로운 치료법에 대한 추가 연구가 필요했습니다.
관련 연구 결과는 최근 Journal of Clinical Oncology에 "Phase I Trial of GD2.CART Cells Augmented With Constitutive Interleukin-7 Receptor for Treatment of High-Grade Pediatric CNS Tumors"이라는 제목으로 게재되었습니다.
텍사스 아동암센터 종양학자인 빌랄 오머(Bilal Omer) 박사는 “뇌종양은 면역억제력이 뛰어나 CAR-T 세포를 효과적으로 차단할 수 있다”며 “우리의 목표는 C7R이라는 수용체로 GD2를 조작해 이를 수행하는 것”이라고 말했습다. 이 연구는 이 치료법이 종양에 효과적으로 침투할 수 있으며 C7R을 첨가하면 항종양 활성이 안전하게 향상된다는 것을 보여줍니다."
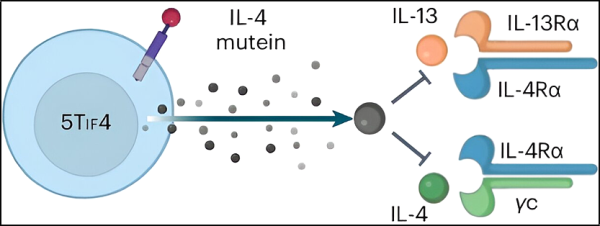
5. Nature Immunology:A single infusion of engineered long-lived and multifunctional T cells confers durable remission of asthma in mice
새로운 연구에서 중국 칭화대학교 연구진은 유전자 변형된 수명이 긴 다기능 T 세포가 생쥐의 알레르기성 천식 징후와 증상을 최대 1년 동안 억제한다는 사실을 발견했습니다. 특히 그들은 제2형 고증상 천식과 관련된 인터루킨의 기능을 감소시키기 위해 CAR-T 세포를 유전적으로 조작했습니다. 관련 연구 결과는 Nature Immunology 2024년 6월호에 게재되었습니다.
이 논문의 제목은 "A single infusion of engineered long-lived and multifunctional T cells confers durable remission of asthma in mice."입니다.
Nature Immunology, 2024, doi:10.1038/s41590-024-01834-9
천식은 기도에 염증이 생기고, 좁아지고, 그에 대한 반응으로 부어오르는 질병으로, 폐에서 과도한 점액이 생성되어 호흡이 어려워집니다. 이 질병은 일반적으로 염증을 감소시키는 흡입제로 치료됩니다. 의료 종사자와 환자 모두 더 나은 치료 옵션을 희망합니다. 새로운 연구에서 저자들은 그러한 치료법을 발견했을 수도 있습니다.
이 저자들은 점액 분비 증가를 초래하는 인터루킨-5(IL-5) 유발 호산구 증가증과 종종 연관되는 매우 특징적인 제2형 천식의 증상을 줄이는 데 중점을 두었습니다.
CAR-T 세포는 가장 일반적으로 암 퇴치와 관련이 있습니다. 그러나 그들은 천식과 같은 다른 질환을 치료하는 데 도움이 될 수 있다고 지적합니다. 그들은 IL-5를 표적 도메인으로 사용하고 BCOR과 ZC3H12A를 삭제하여 호산구를 제거할 수 있는 수명이 긴 CAR-T 세포를 설계했습니다. 그들은 이 세포를 불멸의 기능성 IL-5 CAR-T 세포(5TIF)라고 불렀습니다. 그들은 5TIF 세포를 추가로 변형하여 IL-4 및 IL-13 신호 전달을 차단하는 IL-4 뮤테인을 분비할 수 있도록 하여 5TIF4 세포라고 명명했습니다. 천식 모델에서 완전히 면역 능력이 있는 쥐에 5TIF4 세포를 한 번 주입하면 폐 염증이 지속적으로 억제되고 어떤 조절 요법 없이도 천식 증상이 완화되었습니다.
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.