2024년 Nature 소금은 실제로 항암 면역력을 활성화 및 T세포의 항암 능력을 향상시킬 수 있다는 사실을 처음으로 발견했습니다.
페이지 정보
작성자 PnH 조회80회 작성일 24-10-15 16:34본문
이탈리아 후마니타스 연구병원의 엔리코 루글리(Enrico Lugli)가 이끄는 팀[1]과 독일 뮌헨 공과대학교 크리스티나 E. 지엘린스키(Christina E. Zielinski)가 이끄는 연구팀은 유명한 저널인 "2개 " 에 연속해서 두 개의 중요한 연구 논문을 발표했습니다 . .
두 연구 논문은 동일한 결론에 도달했습니다. 소금은 킬러 T 세포의 항종양 면역력을 향상시킬 수 있습니다. 특히 언급할 가치가 있는 것은 엔리코 루글리(Enrico Lugli) 팀이 쥐를 대상으로 고염 식이요법만으로도 T세포의 항암 능력을 강화하고 종양 성장을 억제할 수 있다는 사실도 확인했다는 점입니다.
염화나트륨이 CD8 양성 T세포의 항암 기능에 영향을 미칠 수 있다는 사실을 과학자들이 발견한 것은 이번이 처음인 것으로 알려졌습니다. 이 두 연구는 또한 다양한 관점에서 항암에 있어서 염화나트륨의 잠재적인 메커니즘을 밝혀냈는데, 이는 새로운 면역요법 전략 개발에 큰 가치가 있습니다.
엔리코 루글리(Enrico Lugli) 팀과 크리스티나 E. 지엘린스키(Christina E. Zielinski) 팀은 왜 소금이 T세포의 항암 활성에 미치는 영향을 연구하려고 생각했을까요?
이는 주로 최근 일부 연구에서 염화나트륨(식용소금)이 면역력을 조절할 수 있다는 사실이 밝혀졌기 때문입니다. 예를 들어, 고염식은 박테리아 감염과 싸우는 호중구의 능력을 억제할 수 있으며 [3], 고염식은 장내 세균에 영향을 주어 종양 성장을 억제할 수 있습니다 [4] . 염은 조절 T 세포의 미토콘드리아 호흡을 방해하여 조절 T 세포 기능 장애를 일으킬 수 있습니다.
위 세 가지 연구를 보면 고염이 항종양 면역에 도움이 되는 것 같다(NK 세포의 항암 활성이 증가하고, 면역을 억제하는 조절 T 세포의 활성이 감소)는 것을 쉽게 알 수 있습니다.
아직 알려지지 않은 연구 분야입니다. 이에 따라 두 연구팀은 서로 다른 각도에서 연구를 시작하게 됐습니다. Lugli 팀은 고염식에 중점을 두었고 Zielinski 팀은 체외에서 T 세포에 대한 고염 치료 효과에 중점을 두었습니다. 다음으로는 루글리팀의 연구 결과를 주로 소개하겠습니다.
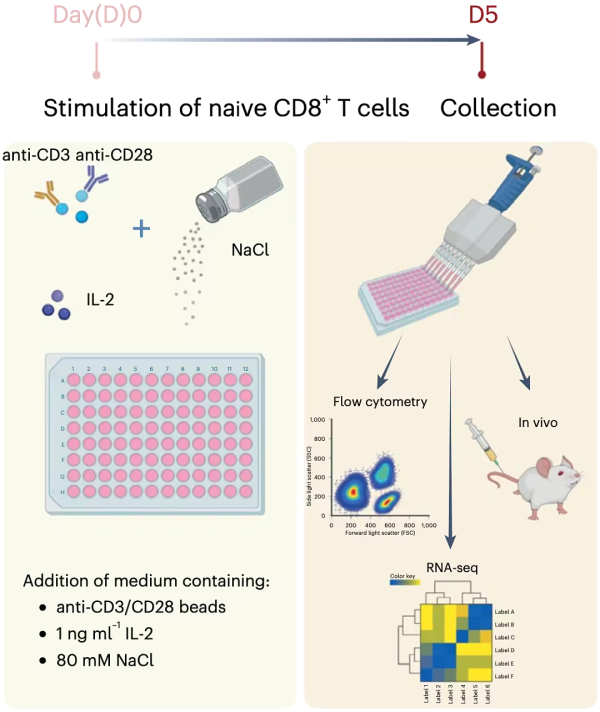
Lugli 팀은 처음에 CD8 양성 순수 T 세포를 고염(80mM)으로 처리했으며(항CD3/CD28 및 IL-2를 추가하여 T 세포를 활성화함), 또 다른 T 세포 그룹을 요소와 만니톨로 처리했습니다. T 세포에 대한 매우 중요한 영향), 고염으로 인한 삼투압 변화를 시뮬레이션하고 대조군으로 사용됩니다.
대조군 세포와 비교하여, 염화나트륨 처리는 그랜자임 B(GZMB) 및 TIM3을 코딩하는 유전자의 발현을 증가시켰는데, 이는 높은 염분이 활성화된 효과기억 T 세포를 유도함을 나타냅니다. RNA 시퀀싱 결과는 또한 대조군과 비교하여 전사체 수준에서 높은 염분 유도 변화와 IFNG, TNF, GZMB 및 TBX21 (T-bet 인코딩)과 같은 효과 또는 세포독성과 관련된 전사체가 상향 조절되었음을 보여주었습니다. FOXO1, RUNX1, SATB1 및 ID3 과 같은 줄기 관련 성적표도 상향 조절됩니다 .
그들은 또한 T 세포 대사 재프로그래밍을 유도하는 원형질막 글루타민 수송체 SLC1A5 및 SLC7A5뿐만 아니라 마스터 조절자 MYC , 해당작용 관련 PKM 및 LDHA를 코딩하는 유전자의 발현도 상향 조절된다는 것을 발견했습니다. 이는 높은 염분이 T 세포 대사를 재형성할 수도 있음을 보여줍니다.
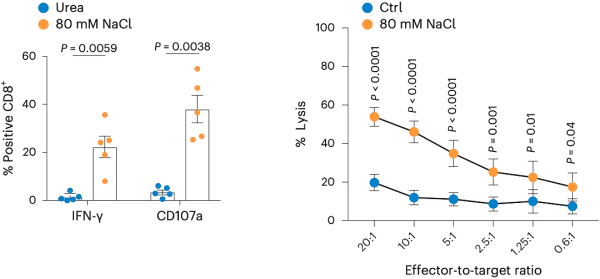
세포 기능의 변화 관점에서 볼 때, 고염 처리는 대조군에 비해 인터페론-γ(IFNγ)와 탈과립 표지자 CD107a의 생성을 증가시켰다. 시험관 내 세포 독성 테스트 결과는 고염으로 처리된 T 세포가 IL-2로 처리된 세포보다 흑색종 세포를 죽이는 데 더 효율적이라는 것을 보여주었습니다. 또한 그들은 T세포 수용체(TCR) 신호 전달이 강화되었으며 고염분이 작용하려면 TCR 활성화 자극과 결합되어야 한다는 사실도 알아냈습니다.
위 연구 결과를 바탕으로 Lugli 팀은 고염이 인간 CD8 양성 T 세포의 이펙터 분화를 촉진할 것이라고 믿고 있습니다.
체외 실험의 지원을 받아 Lugli 팀은 고염식 식단이 생쥐의 항종양 면역에 영향을 미치는지 여부에 대한 대담한 조사를 원했습니다.
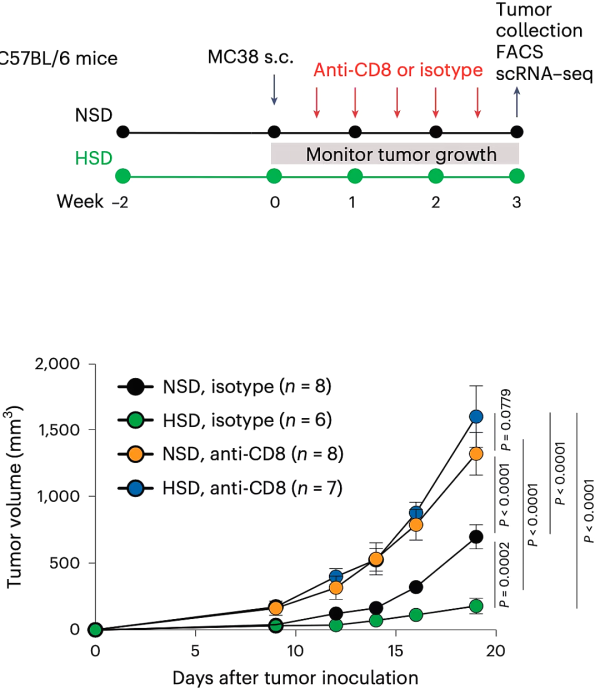
그들은 생쥐에게 고염분 식단(염분 함량이 4%인 음식과 염분 함량이 1%인 물)을 마련하고 생쥐가 자유롭게 먹을 수 있도록 했습니다. 고염식(HSD)을 시작한 지 2주 후, 그들은 MC38 결장 선암종 세포를 쥐에 이식했습니다. 그들은 고염식을 하면 쥐의 전반적인 건강에 영향을 주지 않으면서 염화나트륨이 종양에 축적되고 다른 기관에도 어느 정도 축적된다는 사실을 발견했습니다.
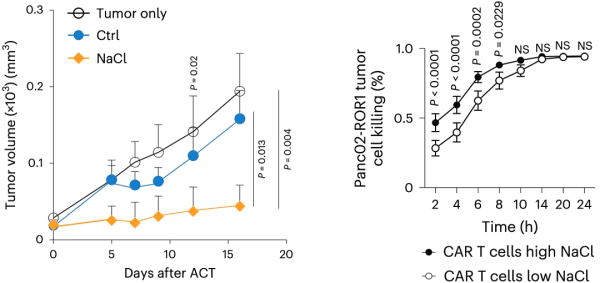
항종양 효과의 관점에서 볼 때, 일반 식단(NSD)에 비해 고염 식단은 종양의 성장을 현저히 억제할 수 있습니다. 그러나 쥐의 CD8 양성 T 세포를 제거하기 위해 항CD8 단클론 항체를 사용한 후에는 고염의 항종양 효과가 완전히 사라질 것입니다. 이는 CD8 양성 T 세포가 고염식의 항종양 효과의 핵심임을 보여줍니다.
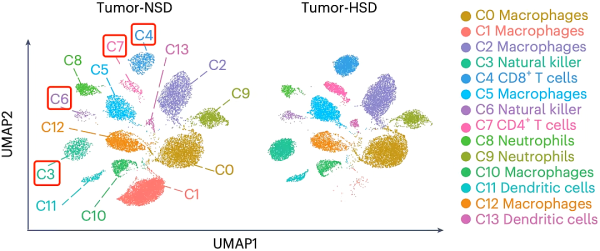
루글리 연구팀은 생쥐 종양의 면역세포 변화를 분석한 결과, 고염식을 한 그룹의 종양에서 CD8 양성 T세포, 자연살해세포, CD4 양성 T세포의 빈도가 2배 이상 증가한 것을 발견했습니다.
특히 CD8 양성 T 세포의 경우 대조군과 비교하여 최종 분화 및 실패와 관련된 전사물(예: Prdm1, Eomes, Maf, Hspa1a 및 Gzmk )은 고염식 그룹에서 감소한 반면, 세포독성 분자 전사물을 암호화하는 전사물은 감소했습니다. 활성화( Tnfrsf9, Nfkb1 ) 및 효과기 분화( Irf8, Csf1, Id2 )와 관련된 전사체 ( Gzmf, Gzme, Gzmd, Prf1 )가 증가했습니다.
고염식 식단이 면역 활성화를 촉진하는 동시에 면역 억제 효과도 제거한다는 사실은 어렵지 않게 볼 수 있습니다. Lugli 팀은 또한 고염식으로 유도된 CD8 양성 T 세포의 변화가 PD-1 억제제로 유도된 변화와 유사하다는 사실을 발견했다는 점에 주목할 필요가 있습니다.
다음으로 Lugli 팀은 고염식 식단이 CD8 양성 T 세포를 개조하는 메커니즘을 조사했습니다.
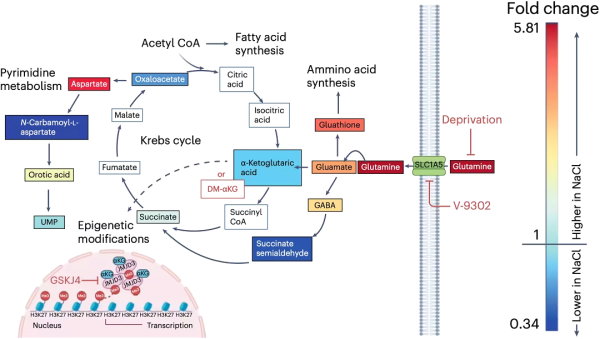
간단히 말해서, 이것은 글루타민 의존적 과정입니다. CD8 양성 T 세포의 고염 처리 후, 글루타민 수송체를 코딩하는 유전자의 발현이 상향 조절되어 글루타민의 흡수가 촉진되어 글루타민이 대사되어 αKG를 생성하고 αKG는 TET 효소 및 JMJD3 효소와 같은 탈메틸화를 활성화합니다. 효소의 증가는 CD8 양성 T 세포의 특정 유전자 부위(예: 효과기 분자 IFNG 및 GZMB 등을 코딩하는 유전자)의 염색질 접근성을 증가시킵니다.
간단히 말해서, 고염식은 CD8 양성 T 세포의 글루타민 흡수를 촉진하여 후생적 수준에서 T 세포를 재프로그램하고 T 세포의 항종양 활동을 강화합니다
Zielinski 팀의 주요 결론은 Lugli 팀의 결론과 유사합니다. 그들은 또한 염화나트륨이 인간 CD8 양성 T 세포의 활성화 상태와 이펙터 기능을 향상시킬 수 있으며 이러한 변화는 대사 능력 향상과 관련이 있다는 것을 발견했습니다.
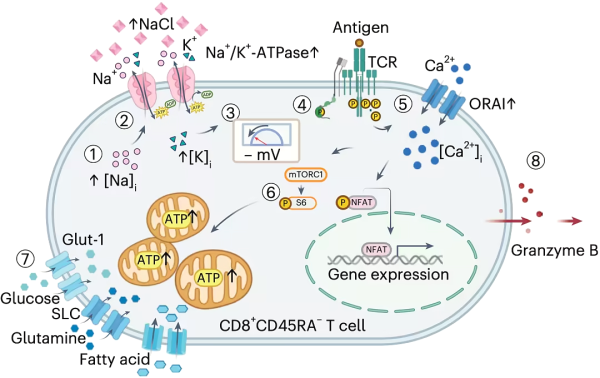
그러나 그 뒤에 숨은 메커니즘 측면에서 Zielinski 팀은 다른 발견을 했습니다. 그들은 높은 수준의 염화나트륨이 CD8 양성 T 세포에서 Na + /K + -ATPase 활성의 상향 조절을 유도하고, 세포막 전위의 과분극을 촉진하고, 세포 내로 Ca 2+ 의 흐름을 증가시키고 , TCR 신호를 증폭시킬 것이라고 믿습니다. T 세포 활성화 및 대사 재프로그래밍을 촉진합니다.
지엘린스키 팀이 발견한 메커니즘은 루글리 팀과 다르지만 서로 충돌하지 않으며 보완적이어야 합니다. 이 두 가지를 종합하면 염화나트륨이 항종양 면역력을 강화하는 메커니즘을 더 깊이 이해하는 데 도움이 될 것입니다.
두 연구 모두 염화나트륨이 항종양 면역력을 향상시킬 수 있다는 것이 입증되었지만 이 결론은 아직 전임상 탐색 단계에 있다는 점을 상기해야 합니다. 이 두 가지 연구를 바탕으로 고염식 식단이 암과 싸우거나 심지어 암을 예방할 수 있다는 결론을 내릴 수 없습니다.
고염식에 임상적 항암 효과가 있는지는 말할 것도 없고, 장기간 고염식을 하면 인체에 미치는 다양한 해로움은 모두가 고염식을 멀리하게 만들기에 충분합니다.
두 연구에서 연구자들은 임상적으로 매우 중요한 연구를 수행했습니다. T 세포를 염화나트륨으로 치료하면 생쥐에서 T 세포 치료의 항암 효과를 향상시킬 수 있다는 것입니다. 이번 발견은 CAR-T, TCR-T 등 T세포 기반 세포면역치료의 간단한 처리를 통해 효능을 높일 수 있을 것으로 기대된다는 의미합니다
1.Scirgolea, C., Sottile, R., De Luca, M. et al. NaCl enhances CD8+ T cell effector functions in cancer immunotherapy. Nat Immunol. 2024. doi:10.1038/s41590-024-01923-9
2.Soll, D., Chu, CF., Sun, S. et al. Sodium chloride in the tumor microenvironment enhances T cell metabolic fitness and cytotoxicity. Nat Immunol. 2024. doi:10.1038/s41590-024-01918-6
3.Jobin K, Stumpf NE, Schwab S, et al. A high-salt diet compromises antibacterial neutrophil responses through hormonal perturbation. Sci Transl Med. 2020;12(536):eaay3850. doi:10.1126/scitranslmed.aay3850
4.Rizvi ZA, Dalal R, Sadhu S, et al. High-salt diet mediates interplay between NK cells and gut microbiota to induce potent tumor immunity. Sci Adv. 2021;7(37):eabg5016. doi:10.1126/sciadv.abg5016
5.CôrteReal BF, Hamad I, Arroyo Hornero R, et al. Sodium perturbs mitochondrial respiration and induces dysfunctional Tregs. Cell Metab. 2023;35(2):299-315.e8. doi:10.1016/j.cmet.2023.01.009
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.