2022년 CAR-T 기술 및 TCR-T 기술 연구보고서
페이지 정보
작성자 PnH 조회152회 작성일 24-05-17 14:37본문
CAR-T (Chimeric Antigen Receptor T-Cell Immunotherapy),즉Chimeric Antigen Receptor T-Cell Immunotherapy .
이 치료법은 수년동안 사용되어 왔지만 최근 몇년동안 임상적으로 개선되고 사용된 새로운 유형의 세포치료법 입니다. 급성 백혈병 및비호지킨 림프종의 치료에 놀라운 효능이 있으며 가장 유망한 종양치료방법으로 확인되었습니다.
모든 기술과 마찬가지로 CAR-T기술도 긴진화과정을 거쳤으며 이러한 일련의 진화과정에서 CAR-T기술이 점차발전해 왔습니다.
이 새로운 치료전략의 핵심은 표적세포를 인식하고 유전적으로 변형된 후 환자의T세포가 이 CAR을 발현하는 키메라항원수용체(CAR)로 알려진 인공수용체 입니다. 임상에서 과학자들은 투석과 유사한 과정을 통해 환자로부터 일부T세포를추출한다음 실험실에서 이를 유전적으로 변형하여 이T세포가 이새로운수용체를 발현 할수있도록 이CAR을 암호화하는유전자를 도입합니다. 이유전적으로 변형 된 T세포는 실험실에서 배양후 환자에게 다시주입됩니다.
이러한T세포는 표적세포표면의 분자에 결합하기위해 발현하는 CAR수용체를 사용하고 ,이결합은 내부신호를 유발하여T세포를 매우강력하게 활성화 시켜 표적세포를 빠르게파괴합니다.
최근에는 급성백혈병 및 비호지킨림프종치료에 사용되는것 외에도 CAR-T면역요법이 개선되어 고형종양,
자가면역질환, HIV감염 및 심장질환과 같은 질병치료에 도적용범위가 넓어지고 있습니다.
1. 혈액암: CAR-T세포치료후 재발한 다발성골수종환자의 치료의 핵심을 밝혀낸 새로운 연구
새로운 연구에서 Mount Sinai의Icahn School of Medicine과Memorial Sloan Kettering Cancer Center의 연구원들은CAR-T세포치료 후 암이재발한 다발성골수종환자를 도울수있는치료법을 확인했습니다. 관련 연구결과는
2022년11월3일Blood저널에 온라인게재될예정입니다.
논문제목은"Interventions and results of multiple myeloma patients getting save treatment after BCMA-directed CAR T therapy"입니다.
새로운 연구에서 저자는 BCMA-표적화라고하는 일종의CAR-T세포요법으로 치료한후 재발했을때 여러가지 다른치료를받은 다발성 골수종환자의 대규모그룹을 연구했습니다. 이 CAR-T세포요법은 다발성골수종과 싸우기위해 암성형질세포표면의BCMA단백질을 표적으로합니다.
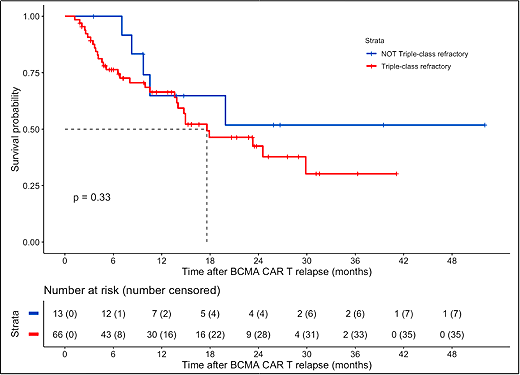
BCMA표적CAR-T세포요법으로치료한 후 암재발까지의 시간
연구에서는 이중특이성항체 및 다른유형의 CAR-T세포요법을 포함한 다른T세포 기반요법이 이러한재발환자에서 가장오랜기간동안 암을 억제하는데 가장 극적인성공을 거둔것으로 나타났습니다.
논문 교신 저자인Mount Sinai의Icahn School of Medicine의Samir Parekh박사는
"이 새로운연구의결과는 CAR이후 악화된환자의결과를 개선하기 위한 향후전향적 임상연구의기초를 제공할것입니다. BCMA표적 CAR-T세포요법으로 치료한후 암이 재발한 대규모코호트환자에게 제공된 다양한치료요법의결과에 대한 첫번째 보고서 입니다. 따라서 골수종환자에 대한 혈액학계의 관심은 매우 흥미롭습니다."
2. 임상1상시험에서 CRISPR로 편집된 범용CAR-T세포가 재발성B세포 백혈병치료에 사용될수있음을 보여줍니다.
새로운임상연구에서Great Ormond Street Children's Hospital과University College London의연구원들은CRISPR/Cas9기술을 사용하여 기증자의 T세포를 유전적으로 변형하여 약물내성 백혈병을 앓고 있는 위독한
소아암환자를 치료했습니다. 소아암환자들은 가능한 모든치료법을 시도해봤습니다. 이1상임상시험은 인간에게 CRISPR유전자편집으로 T세포를 사용한 최초이며 암치료를위해 유전자편집 세포를 사용하는데있어 중요한
진전을 나타냅니다. 이 임상시험의 일환으로 보다정확한 게놈편집 T세포의 새로운세대를 구성하고 적용했습니다. 관련연구결과는 2022년10월26일Science Translational Medicine저널에 게재 되었습니다.
논문제목은 "불응성B세포백혈병 소아치료를 위한CRISPR-engineered CAR19범용 T세포의 임상1상시험"입니다.
저자는 크리스퍼(CRISPR)를 이용해 T세포를 유전적으로 변형했는데, 구체적으로는 T세포의 DNA를 잘라유전자코드조각을 삽입합니다. 이 경우 유전자코드는 T세포가 암성B세포 표면의CD19라는 마커를 인식하는
키메라 항원수용체(CAR)를 발현하도록하고 그결과CD19 CAR-T세포는 이러한암성 B세포를 파괴합니다.
그런 다음 CRISPR을사용하여 CD19 CAR-T세포에서 T세포수용체 α사슬을 파괴하고 CD52를 제거하여TT52CAR19 T세포를 얻었고, 따라서 기증자 일치없이 일반적인 CAR-T세포요법을 구성했습니다
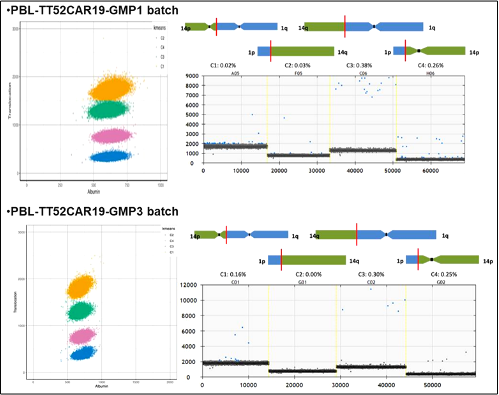
Science Translational Medicine의이미지
14개월에서 11세사이의 재발 및 치료저항성B-ALL어린이6명은 2022년 2월까지 치료를 받았습니다. 이 아이들은모두이전에 B-ALL에 대한 표준치료를 받았지만 불행히도질병이 여러번재발 했습니다. 환자들은 약4주후에
활성화될것으로 예상되는 TT52CAR19 T세포를받았습니다. 이 시간은 암이 현저하게 감소하거나 감지할수없는상태로관해를 달성하기에 충분하다고 판단했습니다. 일단 성공하면 환자는 건강한면역체계를 재건하는데 도움이되는 골수 세포이식을받을수있습니다.
TT52CAR19 T세포로 치료 받은 처음6명의 어린이중4명이 28일이내에 완화되어 조혈줄기세포이식을 받을수있었습니다. 이4명의 어린이중 2명은 치료후 각각9개월과 18개월 동안차도상태를 유지했고 ,불행하게도
나머지2명은 조혈모세포 이식후 재발했습니다. 이새로운 임상연구에서는 병원에서 전반적인 부작용이 예상되고통제되었으며 한명의 어린이가 단기집중치료가 필요했습니다.
3. Cancer Immunol Res:종양대식세포를 표적으로하는 CAR-T세포는 다양한 고형종양을 치료 할것으로예상됩니다
새로운연구에서 미국Mount Sinai의Icahn School of Medicine의연구원들은 새로운 암면역요법이 암을 직접공격하는 대신하나의 면역세포를 사용하여 다른면역세포를 죽이는것을 연구했습니다 .전임상질병모델에서
췌장종양 관련연구결과는2022년11월1일자Cancer Immunology Research저널에게재되었습니다.
논문제목은"Targeting Macrophages with CAR T Cells Delays Solid Tumor Progression and Enhances Antitumor Immunity"입니다.
대부분의 고형종양은 대식세포라고하는 다른유형의 면역세포에 의해 심하게 침윤됩니다. 대식세포는T세포가 종양조직에 들어가는것을 막아서 종양이자라도록 돕습니다. 그러면CAR-T세포와 환자자신의T세포가 암세포를 파괴할수없게 됩니다. 소스에서 이면역억제문제를 해결하기위해 이저자들은 대식세포표면에서분자F4/80을 인식할수있는 "키메라항원수용체(CAR)"를발현하도록T세포를 유전적으로 변형했습니다. 이 CAR-T세포가 종양에
상주하는 대식세포를 만나면 활성화되어 종양에 상주하는 대식세포를 죽입니다.
난소암,폐암 및 췌장종양이있는 실험쥐를 통해이러한 대식세포표적CAR-T세포로 치료하 면종양에 상주하는 대식세포의수가 감소하고 이러한 종양이 줄어들게 됩니다.
종양에 상주하는 대식세포를 죽임으로써 쥐자신의 T세포가 암세포에 들어가 죽일수있게 되었습니다.
저자는 또한 이 항종양면역반응이 이러한CAR-T세포에서 방출되는 염증반응조절에 관여하는 분자인
사이토카인 인터페론에 의해 주도 된다는것을 입증했습니다.
이 논문의 공동교신저자인Mount Sinai의Icahn School of Medicine의Dr. Brian Brown은" 우리의 원래 목표는CAR-T세포를 사용하여 면역억제성 대식세포를 죽이는것 이었지만 ,우리는 그들이 분자를 촉진하여 종양 면역반응 일석이조2마리를 죽이는 단하나의치료법입니다.”라고 말했습니다.
4. 화학요법약물 및CAR-T세포의 효능을 테스트하기위해 3D생체종양모델을 사용한 두개의 논문 비교
Penn State의 연구원들은 전세계적으로 주요 사망원인중 하나인 질병을 더잘이해하기위해 획기적인 연구에서 유방암 종양을 3D바이오프린팅하고 치료했습니다. 이 과학적 최초의 작업은 종양모델의 정확한 생산을 위한
토대를 마련했습니다. 이러한 발전은 동물실험을 사용하지않고 미래 항암요법의 연구개발을 가능하게 할것 입니다.
"이것은 인간면역세포가 고형종양과 어떻게 상호작용하는지 이해하는데 도움이 될것 입니다."라고Penn State의공학 과학 및 역학교수 ,생물의학공학 교수 및 신경외과교수인Ibrahim Ozbolat는 말했습니다. 인간세포와 상호작용하고, 체내에서 전이 및 확산되는지 이해하기 위한 연구플랫폼이기도 합니다."
Ozbolat의연구실은 3D바이오프린팅을 사용하여 인체건강을 위한 다양한조직을 만드는것을 전문으로 합니다. 연구실에서 유방암연구에 도움이되는 3D바이오프린팅사용에 관한두개의 논문이 최근Advanced Functional Materials and Biofabrication저널에각각"Chemotherapeutics and CAR-T Cell-Based Immunotherapeutics Screening on a 3D Bioprinted Vascularized Breast Tumor Model"및"Biofabrication of 3D breast cancer models for dissecting the cytotoxic response of human T cells expressing engineered MAIT cell receptors".

저자들은 비교적 새로운기술인 보조바이오프린팅을 사용하여 종양을 3차원으로 정확하게 찾고조직을 제작했습니다. 그런 다음그들은 이종양조직을 혈관이있는 다단계유방종양모델로 형성했으며 화학요법과 T세포 기반면역요법에 반응하는것으로 나타났습니다. 그들은 먼저 이종양모델을 유방암치료에 일반적으로 사용되는 안트라사이클린화학요법약물인 독소루비신으로 치료하여 정확도를 테스트했습니다. 생체 프린팅 된종양 이화학요법에반응한것을 발견한후 ,그들은 잭슨연구실의면역학자Derya Unutmaz박사와 함께 T세포기반면역요법으로 종양을치료했습니다.
그들은 공격적인유형의 유방암세포를 인식하고 싸우기위해 유전자편집을 통해 조작된인간 CAR-T세포를 사용했습니다. 종양에서 유전자편집된 CAR-T세포를 72시간 동안순환시킨후 ,그들은 생체프린팅된종양의 세포가 활성면역반응을 시작하고 암세포와 싸우고있음을 발견했습니다.
5. 네이처(Nature):“Non-viral precision T cell receptor replacement for personalized cell therapy”
인간의 면역체계는 암세포를 특이적으로 인식하고 정상세포와 구별하는 T세포수용체(TCR)인 T세포표면에 특정수용체를 가지고 있습니다. 이러한 수용체는 환자마다 다르기때문에 이를 분리하고 T세포로 가져와 암에 대한 맞춤형T세포요법을 생성하는 효율적인방법을 찾는것이 이를 가능하게하는 열쇠입니다. .
새로운 연구에서 UCLA와PACT Pharmaceuticals의 연구원들은 처음으로 CRISPR기술을 사용하여 T세포라고 하는 면역세포에 외래유전자를 도입하여 이러한 유전자변형 T세포가 암세포를 공격하는데 집중하도록하여 잠재적으로 정상세포를 손상시키지않고 면역요법의 효과 관련연구결과는2022년11월10일자네이처(Nature)온라인판에"Non-viral precision T cell receptor replacement for personalized cell therapy"라는 논문제목으로 게재될 예정이입니다. 논문의 교신저자는UCLA의Antoni Ribas박사, PACT Pharmaceuticals의Stefanie J. Mandl박사및Susan P. Foy박사입니다.
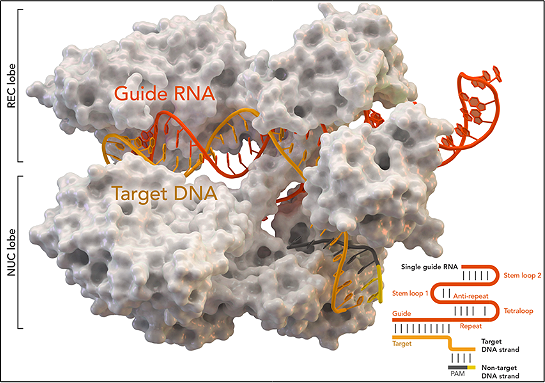
Thomas Splettstoesser(Wikipedia, CC BY-SA 4.0)를통한이미지
CRISPR기술은 이전에 특정유전자를 제거하여 면역체계가 암과 보다효과적으로 싸울수있도록 인간에게 사용되었습니다. 이 새로운연구에서 저자는 CRISPR/Cas9정밀게놈편집을 기반으로 T세포에서 두개의 내인성TCR유전자인 TCRα(TRAC)및 TCRβ(TRBC)를 동시에 제거하고 두개의사슬을 삽입하는 임상등급접근방식을 개발했습니다. TRAC locus에서neoantigen-specific TCR(neoantigen-specific TCR, neoTCR)의사용된neoTCR은 환자자신의 순환하는 T세포로부터 분리되고 ,생성된TCR세포를 neoTCR-T세포라고합니다.
결장암 ,유방암, 폐암 을 포함한 난치성고형암환자16명에게 neoTCR-T세포(NCT03970382)의 1상용량 증량시험에서 최대3가지의 서로다른 neoTCR-T세포주입을 실시했습니다. 각 neoTCR-T세포는 환자별neoTCR. 한환자는
1등급 사이토카인방출증후군이발생했고 한환자는 3등급 뇌염이 발생했습니다. 모든 환자는neoTCR-T세포주입을 받기전에 림프구제거화학요법을 받았으며 화학요법후에 예상되는 부작용이 발생했습니다. neoTCR-T세포
주입을 받은후 5명의환자는 안정적인 질병관리를 보였고 나머지11명의환자는 질병이 진행되었습니다. NeoTCR-T세포는 치료 전내인성TCR을 발현하는T세포보다 높은빈도로 neoTCR-T세포치료후 종양생검에서 검출되었습니다.
6. Cancer Immunol Res:Hypophosphatemia Due to Increased Effector Cell Metabolic Activity Is Associated with Neurotoxicity Symptoms in CD19-Targeted CAR T-cell Therapy
새로운 연구에서 UCLA의 연구원들은 키메라항원수용체(CAR) T세포(CAR-T)요법의 신경학적 부작용의 발생률과중증도가 저인산혈증환자에서 현저히 낮았다고 밝혔습니다. 관련 연구결과는 2022년10월19일자
Cancer Immunology Research저널에 온라인게재 되었습니다. 논문제목은 "저인산혈증으로 인한 증가된 이펙터세포 대사활동이CD19-Targeted CAR T-cell Therapy에서 신경독성 증상과 연관됩니다"입니다.
ICANS(immune effector cell-associated neurotoxicity syndrome)로 알려진 CAR-T세포요법과 관련된 신경독성은 이 요법을 받는환자의 약50%에 영향을 미칩니다. 증상으로는 혼돈, 섬망, 실어증, 운동기능장애, 혼수 등이 있습니다. 심한 경우 발작및혼수상태를 포함하여 생명을 위협하는 사건이 발생 할수있습니다.
"ICANS에 대한치료는 현재 비특이적이고 부작용이 있을 수있는 지지요법 및 스테로이드로 제한됩니다.따라서ICANS발병을 예측하는 능력은 임상의에게 매우 도움이 될것입니다."
7. NEJM:소규모 임상시험에서 GPRC5D를 표적으로하는CAR-T세포가 골수종을 효과적으로 치료할수있음을 보여줍니다.










