2023년 CAR-T TCR-T TILs 연구 보고서 (1)
페이지 정보
작성자 PnH 조회115회 작성일 24-05-26 13:06본문
CAR-T (Chimeric Antigen Receptor T-Cell Immunotherapy), 즉 Chimeric Antigen Receptor T-Cell Immunotherapy .
이 치료법은 수년 동안 사용되어 왔지만 최근 몇 년 동안 임상적으로 개선되고 사용된 새로운 유형의 세포 치료법입니다. 급성 백혈병 및 비호지킨 림프종의 치료에 놀라운 효능이 있으며 가장 유망한 종양 치료 방법 중 하나로 간주됩니다. 모든 기술과 마찬가지로 CAR-T 기술도 긴 진화 과정을 거쳤으며 이러한 일련의 진화 과정에서 CAR-T 기술이 점차 성숙해졌습니다.
이 새로운 치료 전략의 핵심은 표적 세포를 인식하고 유전적으로 변형된 후 환자의 T 세포가 이 CAR을 발현하는 키메라 항원 수용체(CAR)로 알려진 인공 수용체입니다. 임상 시험에서 과학자들은 투석과 유사한 과정을 통해 환자로부터 일부 T 세포를 추출한 다음 실험실에서 이를 유전적으로 변형하여 이 T 세포가 이 새로운 수용체를 발현할 수 있도록 이 CAR을 암호화하는 유전자를 도입합니다. 이 유전적으로 변형된 T 세포는 실험실에서 확장된 다음 환자에게 다시 주입됩니다. 이러한 T 세포는 표적 세포 표면의 분자에 결합하기 위해 발현하는 CAR 수용체를 사용하고, 이 결합은 내부 신호를 유발하여 T 세포를 매우 강력하게 활성화시켜 표적 세포를 빠르게 파괴합니다.
최근에는 급성 백혈병 및 비호지킨 림프종 치료에 사용되는 것 외에도 CAR-T 면역 요법이 개선되어 고형 종양, 자가 면역 질환, HIV 감염 및 심장 질환과 같은 질병 치료에도 적용 범위가 넓어지고 있습니다.
1. Sub-Journal of Science: 새로운 연구에 따르면 CAR-T 세포 요법은 고형 종양 수술 후 잔여 종양 세포를 제거할 것으로 예상됩니다.
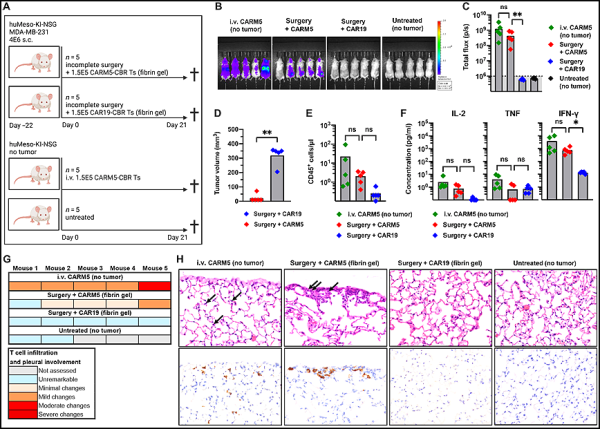
새로운 전임상 연구에서 펜실베니아 대학의 Perelman School of Medicine의 연구원들은 CAR-T 세포 요법이 혈액암을 공격하도록 환자 자신의 면역 세포를 재프로그래밍하는 방법으로 수술 결과를 개선할 수 있음을 발견했습니다. 고형 종양의 치료. 관련 연구 결과는 2023년 1월 13일 사이언스 어드밴시스(Science Advances) 저널에 "Chimeric antigen receptor T cells as adjuvant therapy for unresectable adenocarcinoma"라는 논문 제목으로 게재됐다.
국소적으로 처리된 실험쥐에서 비표적 독성 감소. Science Advances, 2023, doi:10.1126/sciadv.ade2526을 통한 이미지.
새로운 연구에서 그들은 두 가지 유형의 종양 세포의 표면 마커인 메조텔린(mesothelin)이라는 단백질을 표적으로 하도록 CAR-T 세포를 조작했습니다. CAR-T 세포를 포함하는 조작된 피브린 젤을 전달하지 않으면 나머지 종양 조직이 성장했고 쥐는 약 7주 이내에 죽었습니다. 그러나 CAR-T 세포가 포함된 피브린 겔을 투여한 후 20마리 중 19마리의 실험쥐에서 잔존 종양 조직이 빠르게 사라졌고, 이 19마리의 실험쥐는 남은 관찰 기간 동안 상처가 없는 상태를 유지했습니다.
2. JITC: STAb-T 세포 치료제의 활용으로 T세포 급성림프구성백혈병 치료 기대
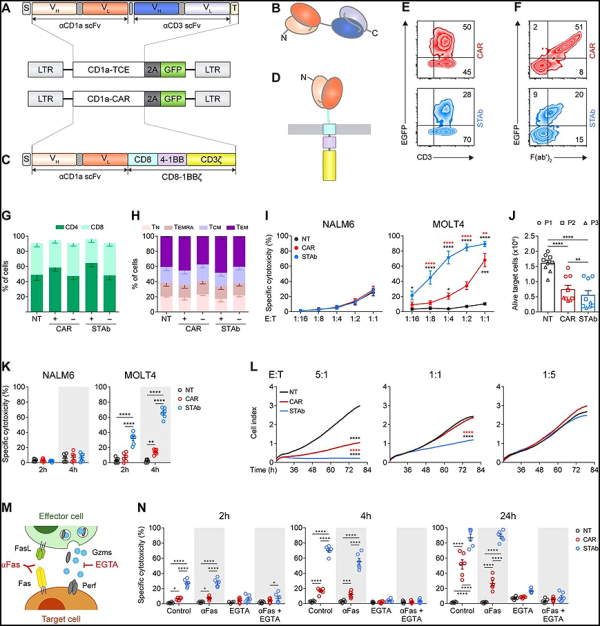
새로운 연구에서 스페인 연구자들은 현재 치료 옵션이 거의 없는 일종의 백혈병에 대한 세포 치료법을 개발했습니다. 이 STAb-T 세포 요법은 STAb-T 세포를 기반으로 하며 화학 요법이나 골수 이식에 반응하지 않는 T-세포 급성 림프구성 백혈병(T-ALL) 환자를 치료할 수 있습니다. 관련 연구 결과는 최근 Journal for ImmunoTherapy of Cancer에 "Efficient preclinical treatment of cortical T cell acute lymphoblastic leukemia with T lymphocytes secreting anti-CD1a T cell Engagers"라는 제목으로 게재되었습니다
CD1a-STAb T 세포와 CD1a-CAR-T 세포의 체외 비교 연구. Journal for ImmunoTherapy of Cancer의 이미지, 2022, doi:10.1136/jitc-2022-005333.
STAb-T 세포 요법은 현재 암 치료에 혁명을 일으키고 있는 CAR-T 세포 요법의 진화입니다. CAR-T 세포 요법은 종양 세포를 인식하고 제거하는 인공 키메라 수용체(CAR)를 발현하기 위해 환자 자신의 면역 세포인 T 세포의 유전적 변형을 기반으로 합니다.
T 세포가 종양 표면의 표적을 인식하는 단일특이항체로 수용체를 발현하는 CAR-T 세포치료제에 비해 STAb-T 세포치료제의 장점은 특수한 형태의 이중특이성 두 개의 표적을 인식하는 항체: 하나는 종양 세포에 있고 다른 하나는 T 세포에 있습니다. 이러한 방식으로 이중특이성 항체는 치료용 T 세포를 종양 세포와 접촉시키는 인공 가교를 형성하여 종양 세포 제거를 촉진하고 건강한 T 세포를 안전하게 유지합니다.
3. PNAS: 사이토카인 결합은 T 세포의 항종양 효능을 향상시킬 수 있습니다.
새로운 연구에서 하버드의 Wyss Institute for Biologically Inspired Engineering, Harvard의 School of Engineering and Applied Sciences(SEAS), Dana-Farber Cancer Institute의 연구원들은 T 세포의 외부 코팅에 흡수되어 통합되는 물질을 사용했습니다.
관련 연구 결과는 최근 PNAS 에 "Cytokine conjugation to enhance T cell therapy"라는 제목으로 게재됐다.
이러한 고정된 사이토카인은 원치 않는 전신 부작용 없이 T 세포 기능을 국소적으로 향상시킵니다. 공격적인 고형 종양인 흑색종이 있는 쥐에서 이 접근 방식은 또한 숙주의 면역 체계를 자극하여 종양 세포와 싸우도록 하여 종양 성장을 억제했습니다. CAR-T 세포 요법을 보완하여 비 치유 세포 용량에서 림프종 종양의 완전한 퇴행을 확인했습니다.
"우리가 본 결과는 고형 종양에 효과적인 ACT와 다양한 혈액암에 대해 더 강력한 ACT를 개발하는 단계를 시사합니다. . 큰 발전입니다. 우리의 방법은 CAR-T 세포를 포함하여 치료 T 세포를 만드는 데 현재 사용되는 프로세스와 쉽게 확장되고 통합될 수 있으므로 임상 적용에 대한 경로가 상대적으로 짧을 수 있습니다."
4. 과학: 합성 IL-2 회로는 면역억제성 고형 종양에서 CAR-T 세포 침투를 촉진합니다
많은 고형 종양은 면역 억제성 미세 환경이 T 세포 침윤, 활성화 및 증식을 방지하기 때문에 T 세포 요법에 반응하지 않습니다. 주요 종양 억제 메커니즘에는 T 세포 수용체(TCR) 신호 전달의 억제와 염증성 사이토카인의 고갈이 포함됩니다. 억압적인 종양 미세 환경을 극복하는 것은 고형 종양 면역 요법의 주요 장애물로 남아 있습니다.
고용량의 IL-2와 같은 염증성 사이토카인으로 T 세포 활동을 보충하면 오랫동안 강력한 항종양 기능을 촉진하는 것으로 여겨져 왔습니다. 그러나 전신 IL-2 요법은 매우 독성이 강하여 모세혈관 출혈 증후군 및 궁극적으로 말단 장기 기능 장애를 포함한 심각한 부작용을 초래하는 것으로 나타났습니다 . 세포 자율적 사이토카인 생산은 사이토카인을 국소적으로 종양에 직접 전달함으로써 이러한 독성을 극복할 수 있는 잠재력을 가지고 있습니다. 새로운 연구에서 UCSF의 연구자들은 종양 특이적 synNotch(합성 노치) 수용체가 IL-2 생산을 유도하는 합성 사이토카인 회로로 치료용 T 세포를 조작했습니다. 이 종양 표적 IL-2 전달 회로는 전신 IL-2 요법의 독성을 최소화하면서 종양 억제를 국소적으로 극복할 수 있는 잠재적인 방법을 제공합니다.
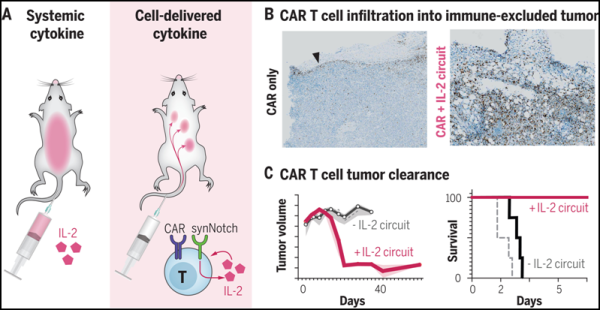
관련 연구 결과는 2022년 12월 16일 사이언스지에 "Synthetic cytokine circuits that drive T cells into immune-excluded tumors"라는 논문 제목으로 게재됐다.
유전자 조작된 치료용 T 세포는 종양이 IL-2 생산을 촉발한 후 면역억제성 종양에 침투하여 제거합니다. Science, 2022의 이미지, doi:10.1126/science.aba1624.
이 저자들은 조작된 synNotch 유도 IL-2 생산 회로(이하 synNotch→IL-2 회로라고 함)가 키메라 항원 수용체(CAR) 또는 TCR T 세포의 면역억제성 췌장암 및 흑색종 에 대한 효율적인 침투를 촉진한다는 것을 관찰했습니다 . 종양 모델. 이러한 도전적인 면역적격 종양 모델에서 이러한 침윤 개선은 종양 제거 및 생존의 실질적인 개선과 관련이 있습니다. IL-2의 전신 전달과 달리 이 국소 IL-2 회로는 TCR/CAR 활성화에 의존하지 않고 여전히 종양을 표적으로 하기 때문에 독성을 나타내지 않습니다.
그러나 IL-2를 전달하는 데 사용되는 정확한 메커니즘이 중요한 것으로 판명되었습니다. IL-2를 구성적으로 발현하도록 조작된 CAR-T 세포 또는 TCR/CAR 유도 IL-2 발현(예: 활성화된 T 세포의 핵 인자(NFAT) 프로모터로부터)과 비교하여, synNotch→IL-2 루프를 운반하는 CAR은 - T 세포는 항종양 효과가 더 좋습니다. 또한, 이 저자들은 동일한 T 세포가 CAR/TCR 및 synNotch→IL-2 회로를 발현하는 IL-2의 자가분비 생산이 중요한 것으로 입증되었음을 발견했습니다. IL-2의 주변분비 전달, 여기서 CAR-T 세포는 경쟁하는 내인성 IL-2 고갈 세포(즉, IL-2 고갈 세포)의 존재 하에서 synNotch→IL-2 회로를 운반하는 독립적인 T 세포에 의해 지원됩니다. - 숙주 조절 T 세포 또는 방관자 T 세포와 같은 - 효과가 없음이 입증되었습니다.
고차원 면역 프로파일링은 이 IL-2 합성 사이토카인 회로가 주로 다른 면역 세포 구획에 눈에 띄는 변화를 일으키지 않고 T 세포 집단에 작용한다는 것을 밝혔습니다. CAR-T 세포와 숙주 방관자 T 세포 모두에 의한 종양 침윤이 상당히 증가했습니다. 그러나 종양과 싸우는 CAR-T 세포만이 활성화, 증식 및 세포 독성의 증가된 마커를 보였고 고갈의 마커는 감소했습니다.
이 저자들은 이 synNotch→IL-2 회로가 TCR/CAR 활성화에 대한 요구 사항을 우회하고 보다 강력한 자가분비 방식으로 IL-2를 전달하기 때문에 효율적이라는 가설을 세웁니다. 따라서 이러한 기능은 조작된 T 세포가 종양 면역 억제 의 주요 모드인 TCR 신호 억제 및 경쟁적 사이토카인 고갈을 극복할 수 있게 합니다 . 이러한 조작된 T 세포는 synNotch에 의해 유도된 IL-2 생산을 통해 종양의 증식을 촉발하는 역할을 한 다음 협력하여 CAR/TCR 매개 영구 T 세포 활성화 및 살상을 개시하는 것으로 보입니다.
5. 과학: CAR-T 세포 표현형을 해독하기 위해 조합 신호 모티프 포인트 학습 사용
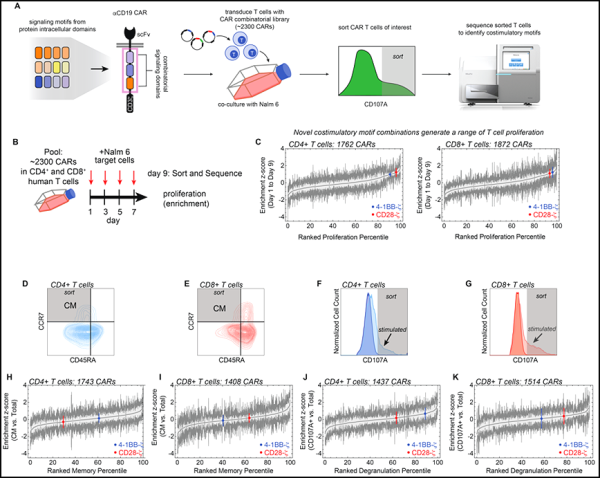
새로운 연구에서 UCSF와 IBM Almaden Research의 연구원들은 조작된 면역 세포가 암 세포를 찾아 끊임없이 죽이도록 지시하는 포인트를 기반으로 하는 새로운 학습 기술을 결합하여 수천 개의 포인트로 구성된 가상 분자 라이브러리를 개발했습니다. 관련 연구 결과는 2022년 12월 16일 사이언스 저널에 게재되었습니다. 논문 제목은 "Decoding CAR T cell phenotype using 조합 신호 모티프 포인트 학습"입니다.
새로운 신호 모티프 조합을 가진 CAR은 풀링된 화면에서 뚜렷한 T 세포 증식, 기억 형성 및 생산 출력을 생성합니다. Science, 2022의 이미지, doi:10.1126/science.abq0225.
이 새로운 연구는 합성 분자가 아닌 기존 분자를 사용하여 세포를 통해 주로 진보를 이룬 분야에 이러한 복잡한 계산 접근 방식을 적용한 최초의 사례를 나타냅니다.
이 새로운 발전을 통해 과학자들은 복잡한 질병을 효과적으로 다루는 데 필요한 정확한 행동을 하기 위해 세포에 어떤 천연 또는 합성 요소를 포함해야 하는지 예측할 수 있습니다.
논문의 공동교신저자이자 UCSF의 Cell Design Institute 소장인 Wendell Lim 박사는 "이것은 이 분야에서 중요한 변화입니다. " 라고 발표했습니다.
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.