2023년 면역세포치료 CAR-T 치료 4월 발표 논문 (2)
페이지 정보
작성자 PnH 조회111회 작성일 24-05-26 18:59본문
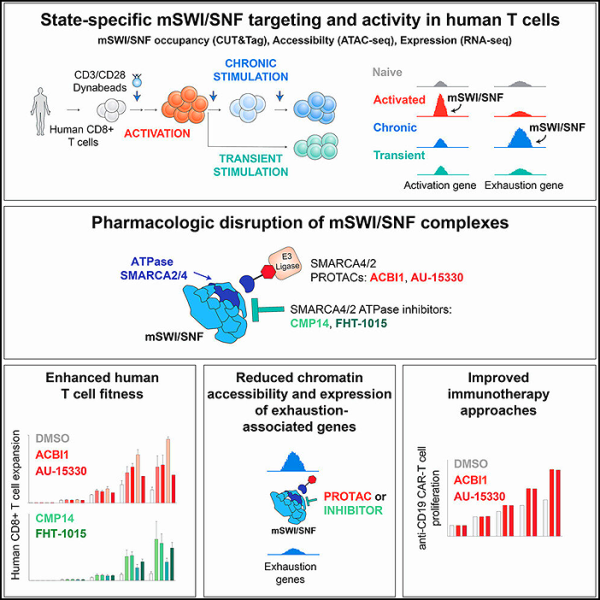
1. Mol 세포: mSWI/SNF 복합체를 표적으로 하는 것은 CAR-T 세포의 감소를 줄이고 암세포에 더 반응하게 유도합니다. T세포의 감소는 암과 싸우는 T 세포에서만 발생하는 것이 아니라 인체 면역결핍 바이러스(HIV), B형 간염 및 C형 간염 바이러스(HBV, HCV), SARS - CoV-2) 와 같은 바이러스 감염 환경에서도 흔히 발생합니다.
Molecular Cell의 이미지, 2023, doi:10.1016/j.molcel.2023.02.026 .
세포 감소로 일부 환자에서 CAR-T 세포 치료의 효과를 약화시켰고 연구원들은 감소의 원인을 찾으려고 노력했습니다. 새로운 연구에서 Dana-Farber Cancer Institute와 NYU Grossman School of Medicine의 연구원들은 우리 세포의 핵에 있는 특수 단백질 세트인 mSWI/SNF(또는 BAF) 복합체를 확인했습니다.이 발견은 CRISPR과 같은 유전자 가위 기술을 통해 표적을 사용하여 세포 감소를 줄이고 CAR-T 세포(및 일반적으로 모든 종양과 싸우는 T 세포)가 지속적인 힘을 갖게 할 수 있음을 시사합니다.
해당 연구 결과는 2023년 3월 20일 Molecular Cell 저널에 온라인 게재되었습니다.
논문 제목은 "Stepwise activity of mSWI/SNF family chromatin remodeling complexes direct T cell activation and exhaustion"입니다.
이 논문의 공동교신저자인 Cigall Kadoch 박사와 Dana-Farber Cancer Institute는 "CAR-T 세포와 살아있는 세포로 만든 기타 치료법은 암과 다양한 기타 질병 치료에 큰 잠재력을 가지고 있습니다. 그러나 이 잠재력을 실현하기 위해 넘어야할 많은 문제와 씨름했습니다. 이 새로운 연구에서 우리의 발견은 이 문제를 해결하기 위한 새롭고 임상적으로 실행 가능한 접근 방식을 제안합니다."
2. NEJM: 임상 시험에서 CAR-T 세포 치료제 Ide-cel이 재발성 다발성 골수종 환자를 치료할 것으로 예상됨
3월은 골수종 인식의 달입니다. 새로운 연구에서 Mayo Clinic Comprehensive Cancer Center의 혈액학자/종양학자인 Sikander Ailawadhi, MD와 동료들은 다발성 골수종 환자에게 더 나은 결과를 제공하는 새로운 개발에 대한 연구를 발표합니다. 관련 연구 결과는 2023년 3월 16일
NEJM 저널에 "Ide-cel or Standard Regimens in Relapsed and Refractory Multiple Myeloma"라는 논문 제목으로 게재되었습니다.
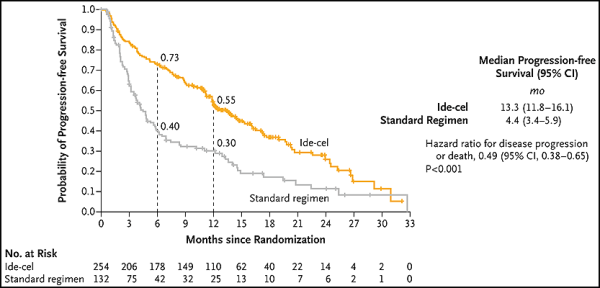
무진행 생존. New England Journal of Medicine, 2023, doi:10.1056/NEJMoa2213614를 통한 이미지.
새로운 연구에서 저자는 이전에 다발성 골수종 치료를 받았지만 치료 후 질병이 재발한 다발성 골수종 환자를 대상으로 CAR-T 세포 치료제인 Ide-cel을 현재 이용 가능한 표준 치료 요법과 비교했습니다. 그들은 무진행 생존율 즉 환자가 아팠지만 악화되지 않은 시간을 치료 과정과 치료 후에 측정했습니다. 이 연구는 중앙값 18.6개월의 환자 추적에서 CAR-T 세포를 받은 그룹에서 무진행 생존 기간이 13.3개월로 표준 치료 그룹에서 4.4개월인 것으로 나타났습니다.
Ailawadhi 박사는 "이러한 발견은 우리가 재발성 다발성 골수종 환자의 치료 과정 초기에 CAR-T 세포 요법을 적용하기 위한 치료계획을 바꾸는 연구로 향하고 있음을 시사합니다. 이는 희망적으로 미래의 표준 치료법이 될 것입니다."라고 덧붙였습니다. "
3. Nat Med: 장내 미생물은 CAR-T 세포 암 면역 요법에서 중요한 역할을 합니다
University of Science, University of South Florida, University of Texas MD Anderson Cancer Center는 장내 미생물이 B세포 림프종 환자의 CAR-T 세포 요법에 대한 반응을 조절할 수 있다는 사실을 발견했습니다. CAR-T 세포 요법 치료를 시작하기 전에 환자의 장내 미생물군집에서 얻은 개인화된 장내 미생물군집 정보는 환자가 이전에 광범위 요법을 받은 적이 없다면 이 요법에 대한 후속 반응을 정확하게 예측할 수 있습니다.
관련 연구 결과는 2023년 3월 13일자 네이처 메디슨(Nature Medicine) 저널에
"A non-antibiotic-disrupted gut microbiome is associated with clinical response to CD19-CAR-T cell cancer immunotherapy"라는 논문 제목으로 온라인 게재됐습니다.
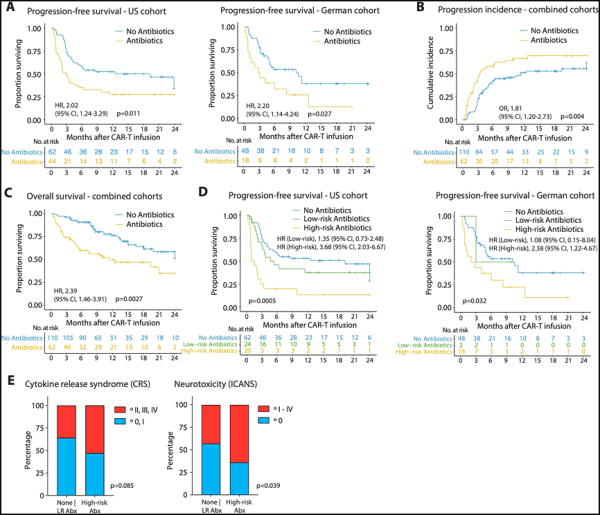
CD19 표적 CAR-T 세포로 치료받은 림프종 환자의 생존 결과 및 독성 부작용에 대한 항생제 노출의 영향. Nature Medicine의 이미지, 2023년, doi:10.1038/s41591-023-02234-6
연구 및 전임상에서 축적된 결과는 장내 미생물이 면역 체크포인트 차단과 같은 T 세포 기반 암 면역 요법의 효능을 조절할 수 있음을 시사합니다. CD19를 표적으로 하는 CAR-T 세포 요법(이하 CD19 CAR-T 세포 요법이라고 함)은 특정 형태의 불응성 및 재발성 B 세포 백혈병 또는 림프종 환자에게 새로운 치료 옵션을 제공합니다. 그러나 면역 요법은 반응의 상당한 이질성으로 인해 방해를 받습니다. 최대 40%의 환자만이 완전하고 장기적인 관해에 도달합니다.
이 새로운 연구에서 저자들은 장내 미생물이 B세포 백혈병 및 림프종 환자에서 CD19 CAR-T 세포 요법의 효능을 조절할 수 있음을 발견했습니다. 가장 규모가 큰 전향적 연구는 CAR-T 세포 요법이 시작되기 전과 시작 후 최대 2년 동안 이전 화학 요법에 실패한 172명의 림프종 환자를 추적했습니다. 흥미롭게도 meropenem, piperacillin-tazobactam 또는 cefepime과 같은 광범위("고위험") 항생제로 치료받은 환자의 20%는 다른 항생제를 받은 환자 및 치료 전에 항생제로 치료하지 않았습니다.
그러나 항생제와 관련된 CAR-T 세포 치료 반응의 감소는 항생제 자체의 효과에 의한 것이 아니라 오히려 CAR-T 세포 치료를 시작하기 전에 "고위험" 항생제를 투여받은 환자를 그렇지 않은 환자와 비교했기 때문입니다. 항생제를 투여받지 않은 환자는 항생제 치료를 받은 환자에 비해 치료 전 종양 부담과 전신 염증이 더 높은 경향이 있었습니다. 이러한 불리한 전처리 조건은 후속 CAR-T 세포 요법의 효과를 떨어뜨립니다.
4. Nat Biotechnol: AI 분석을 통해 급성 골수성 백혈병에 대한 CAR-T 세포 요법의 새로운 표적을 찾았습니다.
급성골수성백혈병은 CAR-T 세포 치료로 효과가 크지 않습니다. 그 이유는 특정 면역 세포가 AML 세포를 특이적으로 표적으로 삼아 면역 체계가 암을 공격할 수 있도록 하는 특정 분자 표적이 없기 때문입니다.
이제 새로운 연구에서 Sebastian Kobold 교수와 Adrian Gottschlich 박사와 독일 뮌헨 대학 병원 임상 약리과의 연구팀, Helmholtz Institute for Health Artificial Intelligence의 Carsten Marr 박사와 Moritz Thomas 박사 뮌헨과 그들의 연구 팀은 이러한 분자 표적을 발견하는 데 성공했습니다.
관련 연구 결과는 2023년 3월 13일자 Nature Biotechnology 온라인판에 게재되었습니다. 논문 제목은 "Single-cell transcriptomic atlas-guided development of CAR-T cells for the treatment of acute myeloid leukemia"입니다.
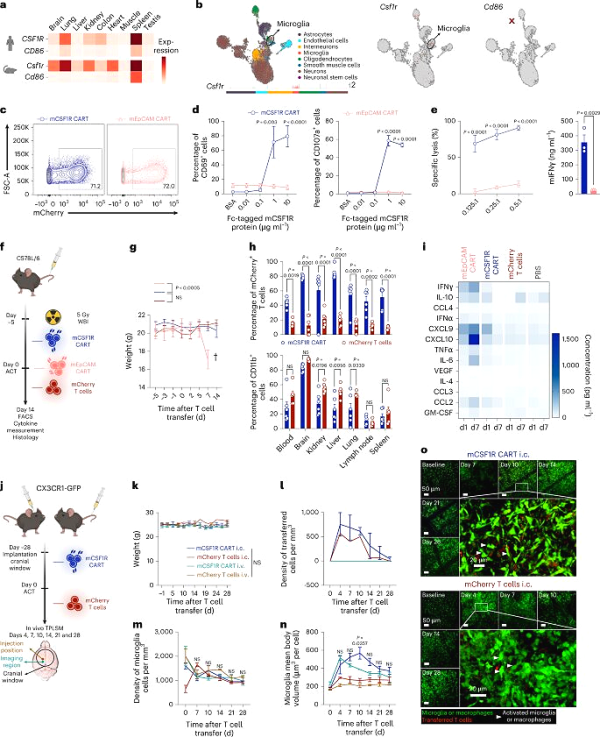
Nature Biotechnology, 2023, doi:10.1038/s41587-023-01684-0을 통한 이미지.
CD19를 표적으로 하는 승인된 CAR-T 세포는 CD19가 (일반적으로) AML 세포의 표면에 존재하지 않기 때문에 AML에 적합하지 않습니다. 연구자들에 따르면, AML 세포의 다른 표면 분자를 표적으로 하는 CAR-T 세포의 임상 결과는 지금까지 암울했습니다. 이는 CAR-T 세포가 건강한 세포와 퇴화된 세포를 구분하지 못하여 그에 따른 심각한 부작용을 일으키기 때문이었습니다.
저자는 AML 세포 표면에서만 이상적으로 발견되는 대체 분자를 찾기 시작했습니다. 광범위한 생물 정보학 분석의
도움 과 500,000개 이상의 세포의 발현 데이터를 통합하여 25,000개의 잠재적인 세포 표면 분자 중에서 2개의 후보 단백질 분자(CSF1R 및 CD86)를 스크리닝했습니다. "몇 년 전만 해도 필요한 단일 세포 데이터가 최근에야 생성되었기 때문에 그러한 분석이 불가능했을 것"이라고 Marr는 말합니다
그런 다음 이 세포를 환자의 AML 세포를 포함하여 다양한 AML 모델에서 테스트했습니다. "한편으로 이러한 CAR-T 세포는 AML에 효과적이며 다른 한편으로는 건강한 세포를 거의 파괴하지 않습니다."
5. JITC: 종양 혈관 정상화 는 교모세포종과 같은 고형 종양에 대한 CAR -T 세포의 효능을 향상시킬 것으로 예상됩니다.
새로운 연구에서 매사추세츠 종합 병원과 미국의 다른 연구 기관의 연구원들은 고형 종양의 혈관 이상을 교정하는 약물이 CAR-T 세포의 전달과 기능을 향상시킬 수 있음을 발견했습니다.
관련 연구 결과는 2023년 3월 10일 Journal for ImmunoTherapy of Cancer 온라인에
"Anti-VEGF therapy Improves EGFR-vIII-CAR-T cell delivery and efficity in syngeneic glioblastoma model in mice"라는 제목으로 게재됐습니다.
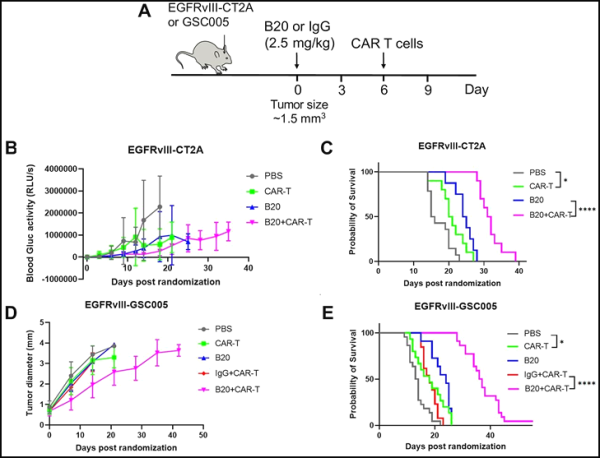
항-VEGF 치료는 마우스 GBM 종양 모델에서 EGFRvIII-CAR-T 세포의 효능을 향상시켰습니다. Journal for ImmunoTherapy of Cancer의 이미지, 2023년, doi:10.1136/jitc-2022-005583 .
논문 교신저자이자 매사추세츠 종합병원 종양생물학연구소장인 Rakesh K. Jain 박사는 "CAR-T 세포 요법이 고형 종양에 효과가 없는 주된 이유 중 하나는 정맥으로 투여되는 CAR -T 세포는 종양의 침윤성 가장자리 또는 종양의 제한된 영역으로만 이동할 수 있습니다.또한 종양은 주변에 면역 억제 미세 환경을 만들어 CAR-T 세포 요법 및 정맥을 통해 전달되는 기타 약물로부터 보호합니다."
Jain과 동료들은 이전에 원래 새로운 혈관의 성장을 억제하기 위해 개발된 항혈관신생 약물로 종양의 혈관을 "정상화"하면 신체의 자연적인 새로운 혈관 생성을 향상시킬 수 있음을 보여주었습니다.
"그래서 우리는 중요한 혈관 신생 분자인 혈관 내피 성장 인자(VEGF)를 차단하는 항체를 사용하여 교모세포종 혈관을 정상화할 수 있는지 조사하여 CAR-T 세포의 침투를 개선할수 있습니다."
6. Adv Mater: 중국연구 발표 논문에 자기 음파 구동 기반의 CAR-T 세포 마이크로로봇을 개발하여 정밀한 새로운 항종양 면역요법 개발에 도움이 될 것으로 기대됩니다.
최근 국제학술지 Advanced에 논문 자료에 "Magnetic-acoustic Sequentially Actuated CAR T cell Microrobots for Precision Navigation and in‐situ Antitumour Immunoactivation"이라는 제목의 연구 보고서에서 Shenzhen Institutes of Advanced Technology, Chinese Academy of Sciences 및 기타 기관의 연구원들은 CAR 기반 T 세포 마이크로 로봇을 개발했습니다. (M-CAR T)은 단일 클릭 접합 기술을 사용하여 CAR-T 세포에 면역 자기 비드를 장착하여 종양 부위를 자율적으로 탐색하고 세포 면역 요법에 반응할 수 있습니다.
중국 과학자들은 자기음향학으로 구동되는 CAR-T 세포 마이크로로봇을 개발했으며, 이는 정밀하고 새로운 항 종양 면역요법을 개발하는 데 도움이 될 것으로 기대됩니다 .
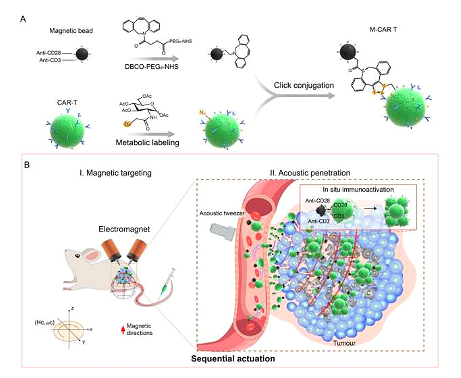
M-CAR T는 CAR-T 세포는 고형 종양의 임상 적용에 큰 희망을 가져오고 미래의 암 면역 요법에 특화된 치료를 전망하고 있습니다.
7. PNAS: "(combination boxing)" 방법은 T 세포를 최소 10배까지 확장할 수 있으며, 이는 고형 종양 치료에서 CAR-T 세포의 효능을 향상시킬 것으로 예상됩니다.
새로운 전임상연구에서 , 미국 펜실베니아 출신 대학의 Perelman School of Medicine의 연구원들은 T 세포가 고형 종양을 공격하는 데 도움이 되는 "combination boxing" 접근법을 제공하는 것을 목표로 합니다. 그들은 염증과 관련된 유전자의 기능을 제어하는 2개의 표적으로 전임상 모델에서 T 세포를 최소 10배 확장시켜 항종양 면역 활동과 지속성을 증가시키는 것을 발견했습니다.
관련 연구 결과는 2023년 3월 15일 PNAS 저널에 게재되었습니다. 논문 제목은 "Combinedruption of T cell inflammatory Regulators Regnase-1 and Roquin-1 enhances antitumor activity of engineered human T cells"입니다.
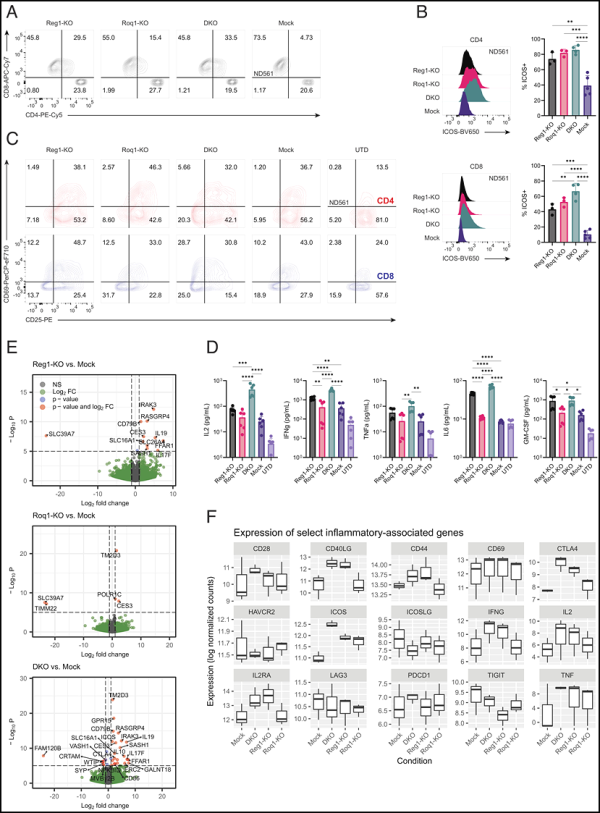
PNAS의 이미지, 2023, doi:10.1073/pnas.2218632120
Regnase-1 및 Roquin-1 이중 녹다운은 조작된 T 세포의 활성화 프로파일을 변경합니다.
이전의 관찰 연구에서는 염증 조절제 Regnase-1이 T 세포에서 파괴될 때 과도한 염증을 유발하여 재활성화하여 항종양 반응을 일으킬 수 있기 때문에 T 세포 감소의 영향을 간접적으로 극복할 수 있는 잠재적인 표적이라고 제안했습니다. 이 저자들은 Roquin-1과 관련이 있지만 독립적인 조절자를 동시에 표적으로 삼아 항종양 반응을 더욱 강화할 수 있다는 가설을 세웠습니다.
이 저자들은 CRISPR-Cas9 유전자 편집 기술을 사용하여 메소텔린을 표적으로 하는 M5 CAR(mesoCAR) 및 NY-ESO-1(NYESO TCR)을 표적으로 하는 8F TCR --- T에서 Regnase-1 및 Roquin-1의 두 가지 다른 면역 수용체를 제거했습니다. 이 T 세포는 현재 1상/2상 임상 시험에서 연구되고 있습니다.
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.