2023년 면역세포치료 6월 주요 발표
페이지 정보
작성자 PnH 조회81회 작성일 24-05-30 14:57본문
1 JCI: 항암 소토라시브에 대한 폐암 내성의 분자 메커니즘을 규명
스페인 종양학회(SEOM)가 발표한 최신 데이터에 따르면 2023년 스페인에서 30,000건 이상의 새로운 폐암 사례가 발생할 것이며, 이로 인해 폐암이 스페인 인구에서 두 번째로 흔한 암 유형입니다. 발병률 외에도 이 유형의 암 환자의 5년 생존율도 모든 암 유형 중에서 가장 낮습니다.
최근 국제학술지 Journal of Clinical Investigation 에 게재된 "Kras oncogene ablation prevent resistance in advanced lung adenocarcinoma"라는 제목의 연구 보고서에서 스페인 국립 암 연구 센터 및 기타 기관의 과학자들은 폐암의 원인을 규명했습니다. 저항의 분자 메커니즘 소토라십 요법에. 각 종양의 특정 생물학을 표적으로 하는 개별화된 치료법은 암세포 성장 및 생존과 관련된 유전자 및 단백질을 특이적으로 표적으로 삼을 수 있는 능력 덕분에 최근 수십 년 동안 암 연구에서 크게 발전한 것 중 하나입니다. 폐암의 경우, 이 돌연변이 유전자를 표적으로 하는 개별화된 치료법은 폐암 환자 치료에 큰 돌파구가 될 수 있습니다.
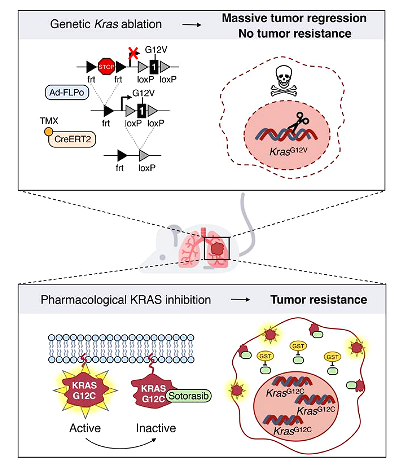
Journal of Clinical Investigation (2023) DOI: 10.1172/JCI164413
폐암에서 가장 흔한 KRAS 돌연변이(흡연의 직접적인 결과)를 표적으로 하는 최초의 개별화 약물인 소토라시브가 미국에서 승인되었으며, 특히 소토라시브는 돌연변이를 억제할 수 있습니다.
KRASG12C isoform, 스페인에서는 매년 약 3,000명의 새로 진단된 폐암 환자가 이 요법의 혜택을 받을 수 있습니다. 그러나 대부분의 환자는 약물에 대한 내성이 빨리 생기고 치료가 더 이상 효과적이지 않기 때문에 연구자들은 더 나은 예방 전략을 개발할 수 있도록 약물 소토라시브에 대한 폐암 내성이 어떻게 발생하는지 연구하고 있습니다.
2 Cancer Discov: 암이 치료에 대한 저항성을 발달시키는 것을 방지하기 위한 새로운 전략의 확인
최근 "Blocking genomic instability prevent Acquired resistance to MAPK inhibitor therapy in melanoma"라는 제목의 연구 보고서가 국제학술지인 Cancer Discovery 캘리포니아 대학의 과학자들과 기관은 새로운 유형의 임상 및 전임상 연구를 통해 표적 요법에 대한 암 저항의 DNA 뿌리를 확인했으며, 이는 과학자들에게 암 치료의 까다로운 문제를 해결할 것으로 예상할 수 있습니다.
로저 로 연구원은 암이 분자진화를 통해 표적 치료제를 회피하는 능력인 후천적 치료 저항성(acquired therapy resistance)을 퇴치하기 위해 새로운 접근법을 취했다고 밝혔습니다.
잠재적으로 치료를 피하는 새로운 유전적 돌연변이를 생성하는 표적 치료를 시작한 직후 암 게놈이 어떻게 변하는지 이해하기 위해 연구자들은 최근 과학자들이 표적 치료법을 개발할 때까지 효과적인 치료법이 없는 공격적인 형태의 피부암인 전이성 피부 흑색종에 집중했습니다. 전이성 흑색종 환자의 거의 절반에서 발생하는 BRAF 유전자에 돌연변이가 있는 암 환자와 환자에게 존재하는 다른 많은 유형의 일반적이고 매우 치명적인 암을 대상으로 합니다.
3 Mol Cell: 통제되지 않은 염증을 표적으로 삼아 치료에 저항하는 암에 대한 새로운 치료법으로 이어질 수 있습니다.
염증의 조절 장애는 간 키나제 B1(LKB1) 돌연변이가 있는 종양의 진행을 주도하는 핵심 기능이지만 LKB1 돌연변이와 염증 조절 장애를 연결하는 메커니즘은 현재 명확하지 않습니다. 최근 국제학술지 Molecular Cell 에 게재된 "LKB1 control inflammatory potential through CRTC2-dependent histone acetylation"이라는 제목의 연구 보고서에서 Van Andel Institute 및 기타 기관의 과학자들은 특정 유전자 돌연변이가 어떻게 암 발병을 유발하는 염증 캐스케이드를 유도하는지 밝혀냈습니다.
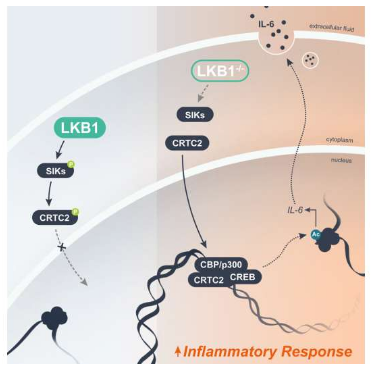
Molecular Cell (2023) DOI: 10.1016/j.molcel.2023.04.017
연구진은 이번 연구 보고서에서 STK11 유전자의 돌연변이가 조절되지 않는 염증을 일으키는 분자 회로를 처음으로 밝혔고, 그로 인한 화학적 데미지는 건강한 세포를 손상시키고 암 발생을 촉진할 수 있습니다. 전통적인 화학 요법과 많은 최신 면역 요법 에 저항하기 때문에 치료할 수 있습니다 . 러셀 존스(Russell Jones) 연구원은 "이 돌연변이가 암을 유발하는 방법과 이유를 이해하는 것은 새롭고 개선된 치료법을 개발하는 데 중요하며, 이번 연구에서 우리는 또한 이러한 암의 중요한 특징을 식별하고 염증을 표적으로 삼으면 종양을 더 많이 만들 수 있음을 보여줍니다.
STK11의 돌연변이는 유전자에 의해 암호화된 지침이 차단되어 유전자가 세포 성장을 통제하는 종양 억제 인자인 LKB1 단백질을 불충분한 수준으로 생산하게 할 때 발생합니다. . LKB1의 돌연변이는 다양한 인간 암, 특히 치료에 내성이 있는 폐암, 췌장암 및 자궁경부암 에서 가장 흔한 유전자 돌연변이 중 하나이며, 희귀 질환인 Peutz-Jeghers 증후군, Peutz-Jeghers 증후군의 주역이기도 합니다. Jeghers 증후군이 있는 사람은 종종 소화관 에 폴립이 발생하며 환자는 암 위험이 상당히 증가합니다.
4 Sci Transl Med: 과학자들은 삼중 음성 유방암 에서 치료에 대한 내성을 극복하기 위한 새로운 잠재적 표적을 식별합니다.
자연 살해 세포(NK 세포)는 종양 미세 환경에 축적되는 세포독성 림프구이며 일반적으로 특정 항종양 특성을 갖는 것으로 간주됩니다. 최근 국제학술지 Science Translational Medicine 에 게재된 "Immature natural killer cells activate progress of triple-negative breast cancer"라는 제목의 연구 보고서에서 마이애미 대학 밀러 의과 대학 및 기타 기관의 과학자들은 연구를 통해 성숙한 자연 살해 세포가 없다는 것을 발견했습니다. 킬러 세포는 삼중 음성 유방암 환자에게 존재할 수 있으며 이러한 유형의 암의 진행을 촉진(억제하기보다는)할 수 있습니다. 이 발견은 특정 NK 세포를 잠재적인 치료 표적으로 식별함으로써 연구원들이 가장 공격적인 형태의 유방암 중 하나인 삼중음성 유방암 환자의 치료에 대한 저항성과 싸우는 데 도움이 될 수 있습니다.
NK세포는 일반적으로 인체의 항 종양면역 . 또한 이 환자 하위 그룹에서 더 나쁜 질병 예후와 관련이 있습니다. 가장 일반적으로 진단되는 인간 암인 유방암은 미국 여성의 암 관련 사망의 두 번째 주요 원인으로 남아 있으며 2020년에만 275,000건 이상의 새로운 사례가 발생했습니다. 전체 유방암의 10~15%를 차지하는 삼중음성유방암은 에스트로겐과 프로게스테론 수용체가 없고 인간표피성장인자(HER2)라는 특정 단백질이 없는 것이 특징이다. 삼중음성유방암 환자는 암의 재발 및 전이율이 높으며, 치료 표적으로서 호르몬 수용체 및 HER2 단백질이 부족하여 현재 이러한 유형의 유방암 환자를 치료할 효과적인 치료법이 없었습니다.
5 PNAS: 과학자들은 표적 치료에 대한 유방암 내성의 분자 메커니즘을 밝힙니다.
재발성 에스트로겐 수용체 양성(ER+) 유방암의 약 4분의 1은 ER 발현이 부족하여 내분비 요법에 내성이 생기고 통제할 수 없게 성장합니다. 최근 베일러 의과 대학 및 기타 기관 과학자들은 국제 저널 Proceedings of the National Academy of Sciences 에 게재된 "14-3-3τ 드라이브 에스트로겐 수용체 손실을 통한 ERα36 유도 및 GATA3 억제 in 유방암"이라는 제목의 연구 보고서에서 암 세포가 어떻게 에스트로겐 수용체를 잃어버리는지 밝혀냈고, 그 과정을 설명하는 데 도움이 될 뿐만 아니라 이를 극복하기 위한 새로운 전략도 제시하는 메커니즘을 밝혔습니다.
연구원인 Weei-Chin Lin 교수는 "수년 동안 우리의 연구 목표는 유방암 진행의 복잡한 퍼즐을 풀고 플레이어가 치료에 대한 저항성과 지속성을 암 세포에 부여하기 위해 어떻게 상호 작용하는지 이해하는 데 도
움을 주는 것"이라고 말했습니다. 이 장애물을 극복하고 이러한 암에서 에스트로겐 수용체 발현을 회복시켜 암이 치료에 잘 적응할 수 있도록 하여 환자에게 더 나은 회복 기회를 제공합니다. 이전에 연구원들은 14-3-3τ 및 ERα36이라고 불리는 두 개의 세포 단백질이 내분비 요법에 대한 유방암의 저항성과 주로 관련되어 있음을 발견했습니다.
인간 에스트로겐 수용체 양성 유방암의 마우스 모델로 작업하면서 연구자들은 이 종양에서 14-3-3τ를 과발현하면 모든 암세포가 에스트로겐 수용체 음성(ER -)이 될 수 있다는 사실에 놀랐다고 Lin 연구원은 말했습니다. 연구 데이터를 본 날을 아직도 기억합니다. 변화는 극적이었고 모든 종양이 에스트로겐 수용체를 잃었습니다. 동물 모델에서 메커니즘을 조사하는 것은 시간이 많이 걸리고 노동 집약적이므로 연구자들은 ER+에서 ER-로의 전환을 더 잘 모방하는 인간 유방암 세포의 회전 타원체 모델인 대체 모델을 개발했습니다.
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.










