2023년 Cell Research 다중 항원 T cell 인식 연구
페이지 정보
작성자 PnH 조회135회 작성일 24-05-31 02:59본문
T 세포 면역요법은 다양한 유형의 암 치료에 혁명을 일으켰습니다.
2023년 7월, 영국 카디프 의과대학 연구진은 Targeting of multiple tumor-associated antigens by individual T cell receptors during successful cancer immunotherapy[1]라는 제목의 연구 논문을 Cell 저널에 게재했습니다.
이번 연구에서는 면역치료를 성공적으로 받은 흑색종 환자에게서 킬러 T 세포가 발견됐습니다. 킬러 T 세포는 "다각적" 방식으로 여러 종양 관련 항원(TAA)을 동시에 인식할 수 있습니다. 이전에 과학자들은 단일 킬러 T 세포가 하나의 항원 표적만 인식할 수 있다고 믿었습니다. 이 슈퍼 T세포는 암 치료의 새로운 길을 제시할 것으로 기대됩니다.
최근 CAR-T 세포 치료의 선구자인 펜실베이니아 대학교 칼 준(Carl June) 교수는 Cell Research 저널에 Swiss Army Knife T cell: one T cell Many Tumor Target[2]이라는 제목의 논문을 게재하고 이에 대해 소개하고 논평했습니다.
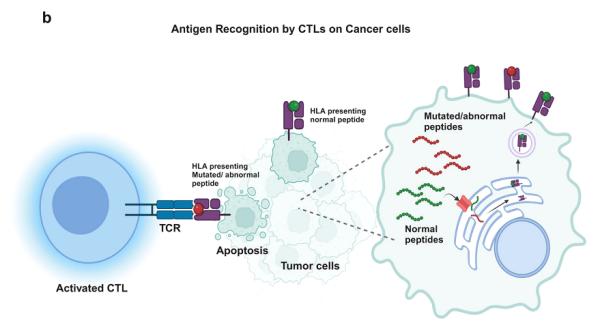
종양 세포에는 종종 돌연변이된 단백질(신생항원)이나 비정상적으로 발현된 단백질(종양 관련 항원)이 있습니다. 항원 제시란 항원이 항원 제시 세포에 흡수되어 면역원성 펩타이드로 소화되는 것을 의미하며, 이는 제시 세포 표면에 펩타이드-HLA 복합체 형태로 제시되고 세포독성 표면의 T 세포 수용체에 의해 포획됩니다. T 림프구(CTL), TCR)은 세포내 병원체, 신생항원 또는 종양 관련 항원에서 생성된 비정상적인 펩타이드를 인식하고 모니터링합니다.
각 T 세포 클론에는 고유한 펩타이드-HLA 복합체를 인식하는 고유한 T세포 수용체(TCR)가 있습니다. 성인의 경우 체내에는 수억 개의 고유한 T 세포 클론이 순환하는 것으로 추정됩니다. 이러한 TCR의 놀라운 다양성으로 인해 T 세포는 수많은 펩타이드-HLA 복합체를 인식할 수 있습니다. 킬러 또는 세포독성 T 림프구(CTL)는 TCR을 통해 표적 세포를 인식할 수 있습니다.
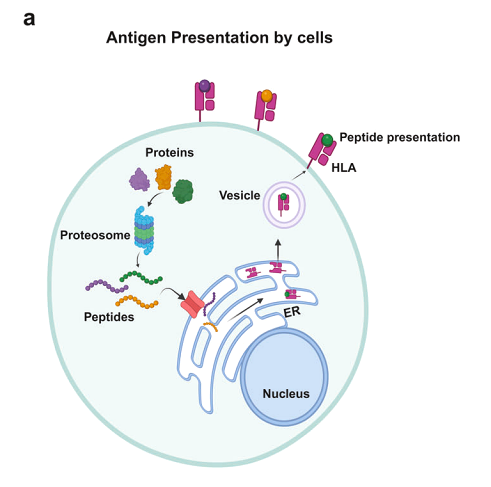
항원 제시 개요, 단백질(항원)은 프로테아좀에 의해 작은 펩티드로 분해된 다음 HLA에 로드됩니다. 일단 로드되면 HLA는 소포체를 떠나 세포 표면에 붙을 수 있습니다.
CTL 세포는 TCR을 통해 비정상 단백질의 펩타이드를 인식하여 표적 세포를 죽입니다.
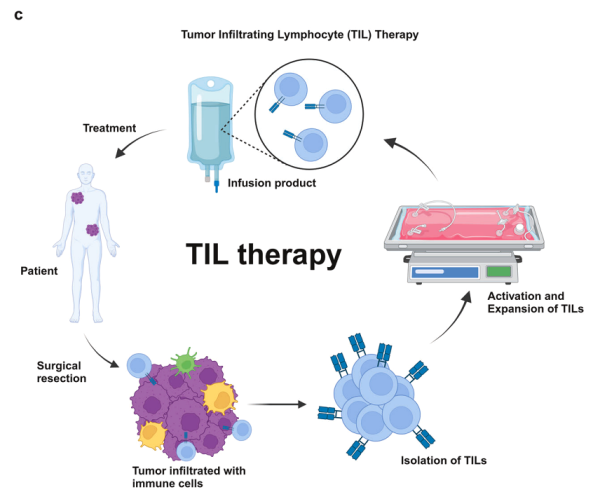
일부 고형 종양에서는 T 세포가 종양 미세환경에 존재합니다. 이들 T 세포 중 일부에는 신생항원이나 종양 관련 항원을 인식하는 TCR이 있습니다. 이러한 종양 특이적 T 세포는 종종 수가 적거나 면역억제성 종양 미세환경에 의해 억제됩니다. 종양침윤림프구(TIL) 치료는 면역세포를 종양에서 분리한 후 배양 해서 활성화 및 확장시키는 면역치료의 한 형태입니다.
TIL 치료 개요
종양침윤림프구(TIL) 요법은 일부 암 환자에서 유망한 결과를 보여 주었으며 관련 임상 시험이 진행 중입니다. TIL이 인식하는 항원, 특히 치료 후 지속적인 완화를 경험하는 환자의 특성을 파악하는 것은 TIL 치료법의 추가 개발에 도움이 될 수 있습니다.
Cell에 발표된 연구에서 Andrew Sewell의 팀은 TIL 면역요법을 성공적으로 받고 10년 동안 암이 없는 상태를 유지한 MM909.24라는 라벨이 붙은 IV기 흑색종을 앓았던 이전 환자를 연구했습니다.
이 환자의 TIL 증폭 세포 중 50%는 배양내에서 흑색종 세포주를 파괴할 수 있었습니다. T 세포는 또한 TCR-HLA 의존적 방식으로 다른 흑색종 세포주를 인식하고 죽일 수 있습니다. T 세포 클론인 MEL8 T 세포가 그의 TIL 세포로부터 분리되었습니다. MEL8 T 세포는 TCR-HLA 의존적 방식으로 흑색종 및 비흑색종 암 세포를 죽일 수 있습니다. 흥미롭게도 MEL8 TCR은 피부 흑색종에서 널리 발현되는 Melan A 단백질에서 유래한 펩타이드를 인식합니다. 비흑색종 세포주는 Melan A 단백질을 발현하지 않기 때문에 항종양 활성의 폭은 놀랍습니다. 흑색종 세포주에서 Melan A 유전자가 제거되었을 때에도 MEL8 T 세포는 여전히 해당 유전자를 죽일 수 있었습니다. 종합하면, MEL8 TCR이 추가적인 종양 관련 항원(TAA)도 인식한다는 것을 보여줍니다.
MEL8 TCR이 인식하는 다른 펩타이드가 무엇인지 확인하기 위해 연구팀은 TAA 펩타이드 데이터베이스를 구축했습니다. 이 데이터베이스를 사용하여 MEL8 TCR은 3가지 다른 TAA(Melan A, BST2 및 IMP2)에서 예측된 상위 10개 펩타이드 중 3개를 식별했습니다.
TCR 교차 반응성은 이전에 입증되었지만 다른 TAA 간에는 나타난 적이 없습니다. 세 가지 TAA 펩타이드가 모두 존재하면 MEL8 T 세포 활성화에 추가 효과가 있습니다. 가장 중요한 것은 Melan A와 BST2 유전자가 제거되어 IMP2만 남게 되어도 MEL8 T 세포는 여전히 종양 세포를 죽일 수 있다는 것입니다.
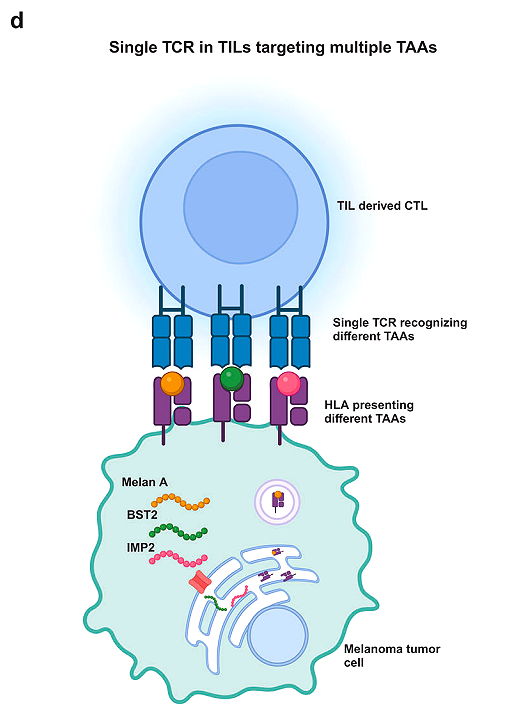
MEL8 T 세포에 의해 발현된 TCR은 3개의 다른 TAA에서 3개의 펩타이드를 인식하여 T 세포 인식을 향상시키고 종양 세포를 사멸시킬 수 있습니다.
일반 인구가 여러 TAA를 인식할 수 있는 T 세포 클론을 가지고 있는지 테스트하기 위해 연구팀은 건강한 개인으로부터 면역 세포를 분리했습니다. 그런 다음 T 세포를 4주 동안 한 번에 하나의 TAA 펩타이드가 로딩된 HLA로 자극했습니다. 이렇게 자극된 T 세포는 단 하나의 TAA에 의해서만 자극되었음에도 불구하고 세 가지 TAA 모두에 결합할 수 있었으며, 이는 대부분의 사람들이 여러 TAA에 대해 면역 반응을 일으킬 수 있는 능력을 가지고 있음을 시사합니다.
종양 관련 항원(TAA)은 돌연변이 단백질이 아니며, 단백질 서열은 정상이나 발현 수준은 비정상입니다. 이는 TAA가 종양 세포에서 높게 발현되지만 정상 세포에서는 낮은 수준으로 발현될 수도 있음을 의미합니다. 이는 잠재적인 오프 타겟 효과 때문에 TAA를 표적으로 삼는 것이 좋은 전략인지에 대한 의문을 제기하며 정상적인 건강한 세포도 세포독성 T 림프구(CTL)에 의해 제거될 수 있습니다.
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.