2025년 nature cancer: An in situ engineered chimeric IL-2 receptor potentiates the tumoricidal activity of proinflammatory CAR macrophages in renal cell carcinoma
페이지 정보
작성자 PnH 조회42회 작성일 25-06-16 12:22본문
이 연구에서는 신세포 암 치료를 위해 현장 조작된 키메라 IL-2 수용체를 통해 CAR-M 세포의 종양 살상 활동을 강화하는 새로운 현장 CAR-M 세포 치료법을 개발했습니다.
산둥대학의 장신이 교수, 스벤캉 교수, 정웨이창 교수 등이 Nature의 자회사 인 Nature Cancer 에 " 현장에서 조작된 키메라 IL-2 수용체는 신세포 암에서 염증성 CAR 대식세포의 종양 살상 활동을 강화한다"라는 제목의 연구 논문을 발표했습니다.
이 연구에서는 신 세포 암 치료를 위해 현장 조작된 키메라 IL-2 수용체를 통해 CAR-M 세포의 종양 살상 활동을 강화하는 새로운 현장 CAR-M 세포 치료법을 개발했습니다 .
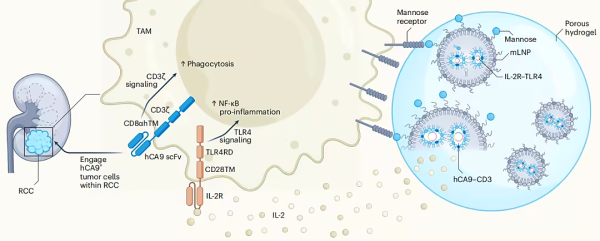
이번 최신 연구에서 연구팀은 키메라 항원 수용체 대식세포(CAR-M)의 염증성 표현형을 조절하고 지속적인 항종양 면역을 강화하기 위해 현장 공학적으로 개발된 키메라 인터루킨(IL)-2 신호전달 수용체(CSR)를 보고 했습니다 .
구체적으로, 연구팀이 맞춤화한 지질 나노입자(LNP)는 이중 원형 RNA를 대식세포에 효과적으로 도입하여 공동 자극 신호 전달 기능을 가진 키메라 항원 수용체-대식세포(CAR-M)를 생성할 수 있습니다. CAR-M의 세포 내 염증 신호 전달 경로는 합성 IL-2 수용체를 통해 IL-2 치료제에 의해 활성화되어 CAR-M이 항종양 표현형으로 전환되도록 유도할 수 있습니다. 신장암 마우스 모델 에서 , 하이드로젤을 이용한 LNP와 IL-2 치료를 병행하면 면역억제성 종양 미세환경이 재형성되고 종양 퇴행이 촉진되었습니다.
전반적으로 이 연구는 CAR-M 세포의 염증성 표현형이 합성 IL-2 수용체에 의해 조절될 수 있음을 보여주며, 이는 CAR-M 세포 치료의 항 종양 면역 요법 에 유익 하며 다른 고형 악성 종양 에 폭넓은 적용 가능성이 있습니다 .
Nature Cancer 저널에서도 "신장암 치료를 위한 생체 내 대식세포 공학" 이라는 제목의 뉴스와 의견 기사를 동시에 게재했다는 점도 언급할 가치가 있습니다 .
이 논문은 CAR-대식세포 치료가 고형 종양의 전임상 모델에서 좋은 활성을 보였다고 지적합니다. 장신이의 연구팀은 CAR 기술과 지질 나노입자(LNP)를 결합하여 생체 내 대식세포 엔지니어링을 위한 플랫폼을 구현했습니다. 이를 통해 지속적인 종양 살상 활동을 하는 염증성 CAR 대식세포를 생성할 수 있었으며, 이는 신세포 암에 대한 효과적인 치료법이 될 것입니다.
T세포가 암호화된 펩타이드를 표적으로 삼아 췌장 종양 세포를 죽일 수 있다는 것을 보여준 것은 이번이 처음입니다.
새로운 연구에 따르면, MIT와 다나-파버 암 연구소의 연구자들은 췌장암 세포에서 발현되는 펩타이드 종류가 T세포 치료 및 췌장 종양을 공격하는 다른 접근법의 유망한 표적이 될 수 있다는 사실을 발견했습니다. 해당 연구 결과는 2025년 5월 8일 Science 저널에 게재되었습니다 .
이러한 분자는 암호화된 펩타이드라고 불리며, 단백질을 암호화하지 않는 것으로 생각되는 유전체의 서열에서 생성됩니다. 이러한 펩타이드는 일부 건강한 세포에서도 발견될 수 있지만, 이번 연구에서 연구진은 췌장 종양에만 존재하는 것으로 보이는 약 500개의 숨겨진 펩타이드를 발견했습니다. 또한 그들은 이러한 신비한 펩타이드를 표적으로 삼는 T 세포를 생성할 수 있다는 것을 보여주었습니다. 쥐를 대상으로 한 연구에서, 이러한 T 세포는 환자 세포에서 유래한 췌장 종양 기관체를 공격하여 종양 성장을 현저히 늦추는 것으로 나타났습니다.
MIT 생물학과 타일러 잭스 교수는 "췌장암은 치료하기 가장 어려운 암 중 하나"라고 말했습니다. "이 연구 는 췌장암 세포의 예상치 못한 약점을 밝혀냈고, 이를 치료에 활용할 수 있을 것으로 기대됩니다."
췌장암은 암 중에서도 생존율이 가장 낮은 암에 속합니다. 진단 후 5년 생존하는 환자는 약 10%에 불과합니다. 대부분의 췌장암 환자는 수술, 방사선 치료, 화학 요법을 병행하여 치료받습니다. 면역 체크포인트 차단 억제제 와 같은 면역 치료법 은 신체의 T 세포가 종양 세포를 공격하도록 자극하도록 설계되었지만 일반적으로 췌장 종양에는 효과가 없습니다. 그러나 임상 시험에서는 변형된 T 세포를 이용해 종양을 공격하는 치료법이 초기 성공을 거두었습니다.
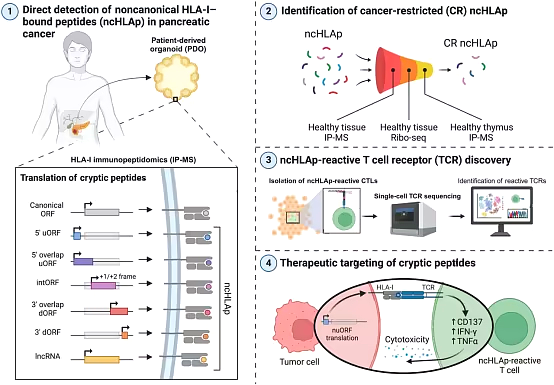
이러한 치료법에는 종양 세포 표면에서 발견되는 특정 펩타이드 또는 항원을 인식하도록 T 세포 수용체(TCR)를 프로그래밍하는 것이 포함됩니다. 가장 효과적인 표적을 찾기 위한 많은 노력이 진행 중이며, 췌장암 유전체의 시퀀싱에서 자주 나타나는 돌연변이 단백질로 구성된 몇 가지 유망한 항원이 발견되었습니다.
새로운 노력에서 연구진은 면역펩티도믹스를 사용하여 췌장암 환자의 조직 샘플로 검색 범위를 확장하고자 했습니다. 면역펩티도믹스는 세포 표면 펩타이드를 추출한 다음 질량 분석법을 사용하여 식별하는 전략입니다. 그들은 약 12명의 환자로부터 췌장 종양 샘플을 사용하여 췌장의 구조를 부분적으로 복제하는 조직의 3차원 성장, 즉 췌장 종양 유기체를 만들었습니다.
브로드 연구소의 제니퍼 에이블린과 스티븐 카가 주도한 면역펩티드 분석 결과, 췌장 종양 기관체에서 발견된 새로운 항원의 대부분이 숨겨진 펩타이드인 것으로 밝혀졌습니다. 이 신비한 펩타이드는 이전에도 다른 종양 유형에서 발견된 적이 있지만, 췌장 종양에서 발견된 것은 이번이 처음입니다. 각 췌장 종양은 평균적으로 약 250개의 숨겨진 펩타이드를 발현했으며, 연구진은 총 약 1,700개의 숨겨진 펩타이드를 발견했습니다.
"데이터를 수집하기 시작하자 이것이 지금까지 가장 풍부한 종류의 새로운 항원이라는 것이 분명해졌습니다. 그래서 우리는 궁극적으로 그것에 집중했습니다."라고 Zackery Ely가 말했습니다.
연구진은 건강한 조직을 분석하여 정상 세포에서도 숨겨진 펩타이드가 발견되는지 확인했습니다. 연구진은 숨겨진 펩타이드의 약 3분의 2가 적어도 한 가지 유형의 건강한 조직에도 존재하는 반면, 나머지 500개 정도는 췌장암 세포에만 국한되어 있는 것으로 보인다는 사실을 발견했습니다. 캘리포니아 대학교 데이비스 캠퍼스의 의학 교수이자 이 연구의 공동 저자인 윌리엄 프리드-패스터는 "이러한 펩타이드는 미래의 면역 치료법에 좋은 표적이 될 수 있다고 생각합니다."라고 말했습니다.
이러한 항원이 T세포 기반 치료법의 표적으로 사용될 수 있는지 시험하기 위해 연구진은 미성숙 T세포를 약 30가지 암 특이 항원에 노출시켰고, 그 중 12가지가 자신을 표적으로 삼는 많은 수의 T세포를 생성한다는 것을 발견했습니다.
연구진은 이러한 T 세포 수용체를 발현하도록 새로운 T 세포 집단을 만들었습니다. 이렇게 조작된 T 세포는 환자의 췌장 종양 세포에서 성장한 오르가노이드를 파괴할 수 있었습니다. 게다가 이러한 기관체를 쥐에 이식한 다음 조작된 T 세포로 치료했을 때 종양 성장이 눈에 띄게 느려졌습니다.
T세포가 암호화된 펩타이드를 표적으로 삼아 췌장 종양 세포를 죽일 수 있다는 것을 보여준 것은 이번이 처음입니다. 연구진은 종양이 완전히 근절되지는 않았지만, 결과는 고무적이었으며 향후 연구에서는 T세포의 살상력이 더욱 향상될 가능성이 있다고 밝혔습니다.
프리드-파스터 연구실은 또한 특정한 숨겨진 펩타이드를 표적으로 삼는 백신 개발에 착수했는데, 이는 숨겨진 펩타이드를 발현하는 종양을 공격하도록 환자의 T 세포를 자극하는 데 도움이 될 수 있습니다. 이러한 백신에는 이번 연구에서 발견된 항원 중 일부가 포함될 수 있습니다.
이 연구는 연구자들이 T 세포 포획 분자와 같은 다른 유형의 치료법을 설계하는 데에도 도움이 될 수 있습니다. T 세포 포획 분자는 한쪽에서는 항원에 결합하고 다른 쪽에서는 T 세포에 결합하는 항체로, 이를 통해 T 세포의 이동 경로를 변경하여 종양 세포를 죽일 수 있습니다. 그들은 잠재적인 백신이나 T세포 치료법이 환자에게 시험되기까지는 몇 년이 걸릴 것이라고 말했습니다.
Zackery A. Ely et al, Pancreatic cancer-restricted cryptic antigens are targets for T cell recognition, Science (2025). DOI: 10.1126/science.adk3487.
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.