2025년 CD4+ T-Cell Lymphoma Harboring a Chimeric Antigen Receptor Integration in TP53
페이지 정보
작성자 PnH 조회33회 작성일 25-02-19 00:05본문
펜실베이니아 대학의 J. Joseph Melenhorst와 Carl H. June이 이끄는 팀이 Nature에 연구 논문을 발표했습니다[1]. 그들은 우연히 T 세포를 수정할 때 CAR이 우연히 TET2 유전자에 삽입되어 유전자 기능 장애를 일으킨다는 것을 발견했습니다. 환자의 몸에 주입한 CAR-T 세포는 증식 능력이 더 강하고, 항암 능력도 더 강하며, 수명도 더 길어졌고, 궁극적으로 환자는 임상적으로 완치되었습니다.
그러나 재발의 원인은 불확실성이 있습니다. 좋은 면이 있으면 나쁜 면이 있는것처럼 불과 4개월 후, Melenhorst와 June의 팀은 Nature Medicine에 또 다른 충격적인 연구 논문을 발표했습니다[2]. 이번에는 CAR-T 세포를 만들던 중 우연히 CAR이 암세포 유전체에 통합돼 'CAR 암세포'가 형성됐고, 결국 환자는 암이 재발해 사망했는 연구발표입니다.
최근 Memorial Sloan Kettering Cancer Center의 Sham Mailankody가 이끄는 연구팀은 최고의 의학 저널인 The New England Journal of Medicine[3]에 드문 사례 보고서를 발표했습니다. 연구팀은 CAR-T 치료를 받은 후 2차 CD4 양성 T세포 림프종 이 발생한 환자의 종양 조직에서 T세포 종양 억제 유전자인 TP53 에 CAR이 통합되는 현상을 처음으로 발견했으며 , 이러한 현상이 2차 T 세포 림프종 의 발생 원인 중 하나 일 것이라고 추측했습니다.
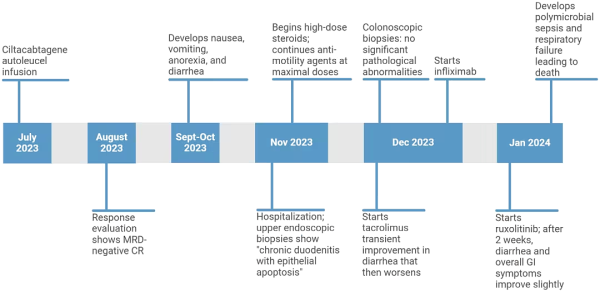
이 연구에서는 내성/재발성 다발성 골수종을 치료하기 위해 자가 BCMA 특이적 CAR-T 세포(ciltacabtagene autoleucel)로 치료받은 72세 여성 환자에 대해 보고했습니다 . 환자는 CAR-T 세포를 주입한 지 1개월 만에 최소 잔류 질환(MRD) 음성으로 완전 관해를 달성했습니다.
그러나 CAR-T 세포 주입 후 약 2개월 후에 환자는 지속적인 메스꺼움, 구토, 식욕 부진, 혈액이 섞이지 않은 물 같은 설사를 겪었고 결국 입원했습니다. 그러나 환자에게는 감염 증거가 없었고 복부와 골반의 CT 스캔에서는 임상적으로 유의한 이상이 발견되지 않았습니다. 상부 내시경 검사와 유연 시그모이드내시경 검사에서도 식도, 위, 근위 십이지장 및 전체 대장에 유의한 이상이 발견되지 않았습니다(두 검사 모두에서 생검 검체를 채취했습니다).
조직 생검 결과, 원인이 알려지지 않은 면역 매개 장염일 가능성이 나타났습니다. 따라서 환자는 다양한 치료 옵션을 받았습니다. 치료 후 환자의 식욕이 개선되었고 설사 빈도도 감소했으며 심지어 퇴원도 가능할 것으로 예상되었습니다. 하지만 퇴원 직전 환자에게 패혈증이 발생하여 결국 사망했습니다.
즉, 의사는 환자의 실제 사망 원인을 알 수 없습니다. 얼마 지나지 않아 병원은 샘플에서 ciltacabtagene autoleucel의 CAR 구조를 검출하기 위한 droplet digital PCR 플랫폼을 구축했습니다. 이 플랫폼의 도움으로 연구자들은 환자의 십이지장 생검 샘플에서 고농도의 CAR을 검출했습니다.
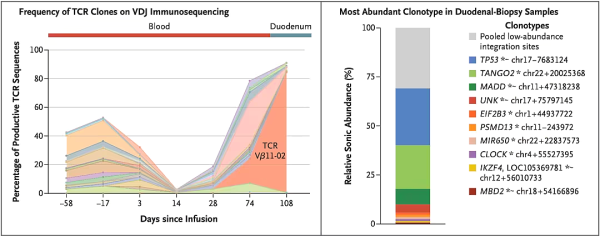
이 발견은 메일란코디 팀의 관심을 끌었습니다. 그래서 그들은 병리학 검사를 다시 시작했습니다. 검사 결과, 환자의 사망 원인은 무증상 CD4 양성 T세포 림프종이나 소화관 림프증식성 질환일 가능성이 있습니다. TCR 서열을 분석한 결과, TCR Vβ11-02 클론이 83.59%를 차지하는 것으로 나타났습니다. 이 클론은 CAR-T 세포 주입 전에는 존재하지 않았다는 점에 주목할 가치가 있습니다. 주입 후 말초 혈액에서의 비율은 28일차에 0.01%에서 74일차에 16.99%로 증가했습니다. 이 CAR-T 세포 클론이 환자의 신체 내에서 엄청나게 확장되었다는 것을 알아내는 것은 어렵지 않습니다.
T 세포 게놈에서 CAR 삽입 부위를 분석한 결과, 두 개의 우세한 부위가 발견되었습니다. 하나는 TP53 유전자 의 첫 번째 인트론 으로 삽입 빈도가 29%였습니다. 다른 하나는 TANGO2 유전자의 첫 번째 인트론으로 삽입 빈도가 23%였습니다. 우리는 모두 잘 알려진 종양 억제 유전자인 TP53 에 대해 잘 알고 있습니다. 연구자들은 조직 샘플에서 p53의 발현을 검출했을 때, 약 90%의 T 세포가 p53 단백질의 발현이 약하거나 전혀 없다는 것을 발견했습니다. TANGO2 도 CAR 삽입이 있지만, 전사와 발현에는 영향을 미치지 않습니다. 또한, 암과 관련이 있다는 연구는 없습니다.
분명히 CAR은 TP53 유전자 에 삽입되어 종양 억제 유전자의 발현을 억제하는데, 이것이 T세포 림프종을 유발하는 주요 원인일 수 있습니다. 그러나 Mailankody 팀은 CD19 표적 CAR-T 세포 치료를 받은 58명의 환자의 데이터를 분석한 후 TP53 유전자 에서 19개의 고유한 통합 부위를 발견했지만 그 중 어느 것도 T 세포의 클론 확장과 관련이 없었습니다. 이는 TP53 의 단일 대립유전자 통합만으로는 CAR-T를 악성 세포로 변형시키기에 충분하지 않을 수 있음을 시사합니다.
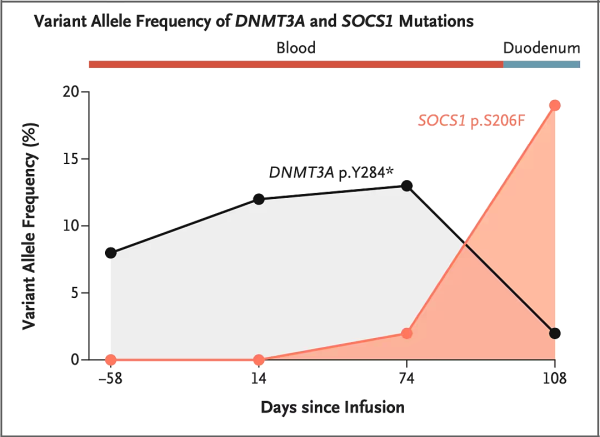
따라서 메일란코디 팀은 T세포의 유전자 돌연변이를 분석하여 JAK-STAT 경로의 음성 조절자인 SOCS1(종양 억제 인자)의 S206F 돌연변이가 주입 시간이 지남에 따라 점차 증가하였으며, TCR Vβ11-02 클론과 시간적으로 일치한다는 것을 발견했습니다. 또한 면역조직화학 분석을 통해서도 JAK-STAT 경로가 활성화된 것이 확인되었고, JAK2 억제제인 룩솔리티닙으로 치료한 후 환자의 2차 임상 증상이 현저히 개선되었습니다.
Mailankody 팀은 위의 연구 데이터를 기반으로, 이 환자의 경우 CAR-T 세포 주입과 CAR 및 TP53 유전자 통합 후에 검출 가능한 SOCS1 유전자 돌연변이가 CAR-T 치료에 따른 CAR 양성 T 세포 림프종의 발생으로 이어질 수 있다고 생각합니다.
추론 논리를 정리해보겠습니다. CAR은 TP53 유전자에 삽입되어 종양 억제 유전자의 발현이 하향 조절되고, 이로 인해 CAR-T 세포가 악성 변형의 잠재력을 가지게 됩니다. 그리고 SOCS1 유전자 돌연변이는 JAK-STAT 신호 전달 경로를 활성화하여 CAR-T 세포의 악성 변형을 더욱 촉진합니다. 마지막으로 TCR Vβ11-02 클론이 급증하여 환자가 사망하게 됩니다. 물론, 그 이면에 있는 분자적 메커니즘은 더 많은 연구와 확인이 필요합니다.
전반적으로 Mailankody 팀은 단 한 건의 분석 데이터만 보고했지만, 이는 CAR-T 세포 치료 후 발생하는 2차 T세포 림프종의 원인이 삽입 돌연변이라는 사실을 뒷받침합니다. 더 중요한 것은 임상 연구자들에게 CAR 통합 방법을 더욱 최적화하고 CAR-T 세포 치료의 장기적인 안전성 모니터링을 실시할 것을 상기시킨다는 것입니다.
1.Fraietta JA, Nobles CL, Sammons MA, et al. Disruption of TET2 promotes the therapeutic efficacy of CD19-targeted T cells. Nature. 2018;558(7709):307-312. doi:10.1038/s41586-018-0178-z
2.Ruella M, Xu J, Barrett DM, et al. Induction of resistance to chimeric antigen receptor T cell therapy by transduction of a single leukemic B cell. Nat Med. 2018;24(10):1499-1503. doi:10.1038/s41591-018-0201-9
3.Perica K, Jain N, Scordo M, et al. CD4+ T-Cell Lymphoma Harboring a Chimeric Antigen Receptor Integration in TP53. N Engl J Med. 2025;392(6):577-583. doi:10.1056/NEJMoa2411507
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.